题目内容
【题目】如图所示的C/Na4Fe(CN)6--钠离子电池是一种新型电池。下列有关说法正确的是
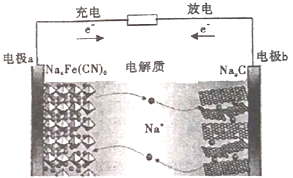
A. 电极a在放电时做正极,充电时做阴极
B. 放电时,电极b上的电极反应为:NaxC-e-=Na++Nax-1C
C. 电池工作时,Na+向电板b移动
D. 该电池通过Na+的定向移动产生电流,不发生氧化还原反应
【答案】B
【解析】分析:原电池中电子从负极流出经外电路流回正极,电解池中,电子从电源负极流向电解池的阴极,电解质中离子定向移动传递电荷,阳极上失去电子,流回电源正极,从图中电池放电电子流动方向知电极b是原电池负极,电极a是原电池正极;从充电时电子移动方向知,a是电解池的阳极,b是电解池的阴极。
详解:结合以上分析A. 电极a在放电时做正极,充电时做阳极,A错误;B. 放电时,电极b上发生氧化反应,电极反应为:NaxC-e-=Na++Nax-1C,B正确;C. 电池工作时,阳离子移向正极,即Na+向电板a移动,C错误;D.电池工作时发生氧化还原反应,D错误;因此,本题答案为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目