题目内容
【题目】溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应。
(1)该反应的化学方程式是__。
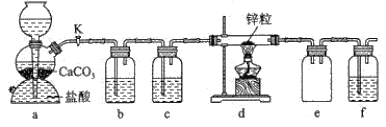
实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操作步骤如下:

①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
已知反应物的用量:0.3molNaBr(s);0.25mol乙醇(密度为0.80g·mL-1);36mL硫酸。
请回答下列问题。
(2)仪器A最好更改为___。
(3)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生。反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的__。
a.饱和食盐水 b.稀氢氧化钠溶液 c.乙醇 d.四氯化碳
(4)本实验的产率为80%,则可制取溴乙烷___g。
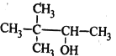
(5)写出由溴乙烷合成乙二醇的路线___。(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
【答案】CH3CH2OH+HBr→CH3CH2Br+H2O 球形冷凝管 a 21.8g CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br![]() HOCH2CH2OH
HOCH2CH2OH
【解析】
(1)制备溴乙烷的一种方法是乙醇与氢溴酸反应生成溴乙烷和水,反应的化学方程式为:CH3CH2OH+HBr→CH3CH2Br+H2O;
(2)实验时,仪器A是直形冷凝管,作用是冷凝回流,可以获得要制取的有机物,为使冷凝效果更好,最好更改为球形冷凝管;
(3)溴单质溶解在有机物中显示棕黄色,为了除去粗产品中的杂质溴单质,可以用氢氧化钠来与之发生反应生成的溶液和溴乙烷互不相溶,故答案为:a;
(4)本实验的产率为80%,则可制取溴乙烷0.25mol×80%×109g/mol=21.8g;
(5)溴乙烷在氢氧化钠的乙醇溶液中加热发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷在氢氧化钠的水溶液中加热发生水解反应生成乙二醇,合成路线为CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br![]() HOCH2CH2OH。
HOCH2CH2OH。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 实验结论 |
A | 向0.1mol/L碳酸钠溶液中滴入酚酞,溶液变红,加热,红色加深。 | 碳酸钠属于弱碱 |
B | 测定醋酸溶液pH,用玻璃棒蘸取溶液,点在pH试纸上,试纸显红色。 | 醋酸溶液显酸性 |
C | 将铜片和锌片用导线相连,插入CuSO4溶液中,锌片质量减小,铜片质量增加。 | 锌被还原 |
D | 向氯化银的浊液中滴入KI溶液,浊液中的固体由白色变为黄色。 | Ksp(AgCl)<Ksp(AgI) |
A.AB.BC.CD.D
【题目】今有室温下四种溶液,下列有关叙述不正确的是( )
序号 | ① | ② | ③ | ④ |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.③和④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B.②和③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C.分别加水稀释10倍,四种溶液的pH:①>②>④>③
D.V1L ④与V2L ①溶液混合后,若混合后溶液pH=7,则V1<V2