题目内容
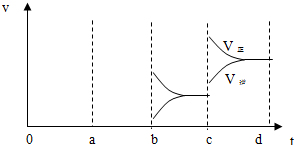
5.在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)?3Z(g)此反应达到平衡的标志是( )| A. | 容器内压强不随时间变化而变化 | |
| B. | 单位时间消耗0.1mol X同时生成0.3mol Z | |
| C. | 容器内X、Y、Z的浓度之比为1:2:3 | |
| D. | 容器内各物质的浓度不随时间变化而变化 |
分析 可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的一系列物理量不变,据此分析解答.
解答 解:A.该反应前后气体物质的量之和不变,则无论反应是否达到平衡状态,则压强始终不变,所以不能根据压强判断平衡状态,故A错误;
B.单位时间消耗0.1mol X同时生成0.3mol Z,方向一致,则不能据此判断平衡状态,故B错误;
C.容器内X、Y、Z的浓度之比为1:2:3,该反应不一定达到平衡状态,与反应物初始浓度及转化率有关,故C错误;
D.容器内各物质的浓度不随时间变化而变化时,正逆反应速率相等,该反应达到平衡状态,故D正确;
故选D.
点评 本题考查化学平衡状态判断,为高频考点,只有反应前后改变的物理量才能作为平衡状态判断依据,为易错题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.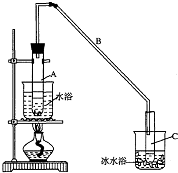 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知: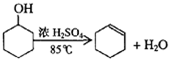
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,
缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是防止暴沸,导管B除了导气外还具有的作用是冷凝.
②试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静 置、分层,环己烯在上层,分液后用c (填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②实验制得的环己烯精品的质量往往低于理论产量,其可能的原因是c
a.蒸馏时从100℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是bc.a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.
 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯已知:

| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,
缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是防止暴沸,导管B除了导气外还具有的作用是冷凝.
②试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静 置、分层,环己烯在上层,分液后用c (填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②实验制得的环己烯精品的质量往往低于理论产量,其可能的原因是c
a.蒸馏时从100℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是bc.a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.
16.下列物质不能溶于Al(OH)3的是( )
| A. | 氨水 | B. | 稀硫酸 | C. | 氢氧化钠溶液 | D. | 浓盐酸 |
20.下列说法不正确的是( )
| A. | 检验Cl-的试剂是硝酸银和硝酸 | |
| B. | 检验SO${\;}_{4}^{2-}$的试剂是氯化钡和盐酸 | |
| C. | 检验CO${\;}_{3}^{2-}$的试剂是盐酸、澄清石灰水和氯化钙 | |
| D. | 向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO${\;}_{4}^{2-}$ |
14.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol氯化钙溶于水配成1 L溶液,所得溶液中Cl-的物质的量浓度为1mol/L | |
| B. | 在标准状况下,11.2LH2O所含的氢原子数为NA | |
| C. | CO2的摩尔质量为44g | |
| D. | 标准状况下22.4LCH4与l8gH2O所含有的电子数均为10NA |
 .
. (1)有下列五种烃:
(1)有下列五种烃: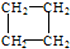 ②
②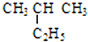 ③乙烷 ④C(CH3)4⑤
③乙烷 ④C(CH3)4⑤ ,其中互为同分异构体的是②④(填序号),②与⑤
,其中互为同分异构体的是②④(填序号),②与⑤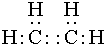 ,E的结构简式为
,E的结构简式为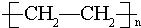 .
.