题目内容
15.利用下列实验装置进行的相应实验,能达到实验目的是( )| A. | 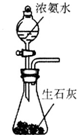 所示装置可制备氨气 | |
| B. | 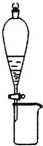 所示装置可分离CH3CH2OH和CH3COOC2H5的混合液 | |
| C. | 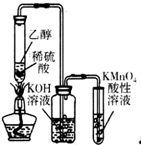 所示装置可制备、收集乙烯并验证其易被氧化 | |
| D. |  所示装置可制取乙酸乙酯 |
分析 A.生石灰与水反应,放出大量的热,可促进氨水挥发;
B.CH3CH2OH和CH3COOC2H5混溶;
C.制备乙烯,应用浓硫酸;
D.应防止倒吸.
解答 解:A.氧化钙与水反应是放热反应,氨气易挥发,可用于制备少量氨气,故A正确;
B.CH3CH2OH和CH3COOC2H5混溶,应用蒸馏的方法分离,故B错误;
C.制备乙烯,应用浓硫酸,且加热到170℃,缺少温度计,故C错误;
D.制备乙酸乙酯,混有乙酸、乙醇,易溶于水,应防止倒吸,故D错误.
故选A.
点评 本题考查化学实验方案的评价,涉及物质的制备、分离、收集等,侧重于学生的分析能力和实验能力以及评价能力的考查,为高考高频考点和常见题型,注意把握实验的方案的合理性和实验操作的合理性,难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
20.下列叙述中指定粒子数目一定大于NA的是( )
| A. | 1mol苯分子中含有双键数 | |
| B. | 1mol CaC2固体中含阴离子总数 | |
| C. | 1L 1mol/L CH3COOH溶液中所含分子总数 | |
| D. | 1mol Cl2参加化学反应获得的电子数 |
7.对下表中实验操作或现象的解释不合理的是( )
| 实验操作及现象 | 现象的解释 | |
| A | 将一片铝箔置于酒精灯外焰上灼烧,铝箔熔化但不滴落 | 单质铝的熔点特别高 |
| B | 用玻璃尖嘴导管导出氢气,点燃,观察到火焰呈黄色 | 普通玻璃中含有钠元素 |
| C | 往水中加入Na2O2固体,滴入酚酞呈红色,振荡,红色褪去 | 产生了碱性物质,且Na2O2具有漂白性 |
| D | 向过量的苯酚浓溶液中滴加少许饱和溴水,振荡,未观察到白色沉淀产生 | 三溴苯酚溶解在过量的苯酚中 |
| A. | A | B. | B | C. | C | D. | D |
4.生活处处有化学.下列说法正确的是( )
| A. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| B. | 煎炸食物的花生油和牛油都是可皂化的饱和酯类 | |
| C. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 | |
| D. | 施肥时,草木灰(有效成分为K2CO3)和NH4Cl混合使用,会产生氨气降低肥效 |
 .
.
 .
.
 .
.