题目内容
【题目】对实验Ⅰ~Ⅳ的实验操作现象判断正确的是( ) 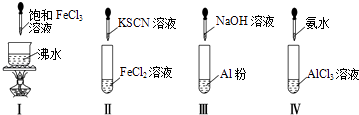
A.实验Ⅰ:产生红褐色沉淀
B.实验Ⅱ:溶液颜色变红
C.实验Ⅲ:放出大量气体
D.实验Ⅳ:先出现白色沉淀,后溶解
【答案】C
【解析】解:A.将氯化铁饱和溶液加入到沸水中加热至溶液呈红褐色可得到氢氧化铁胶体,而非沉淀,故A错误; B.三价铁离子遇硫氰化钾变红色,二价铁离子不变色,故B错误;
C.铝与氢氧化钠溶液反应生成NaAlO2和氢气,有大量气体生成,故C正确;
D.氯化铝与氨水反应生成氢氧化铝白色沉淀,但氢氧化铝不溶于弱碱,故氨水过量时,氢氧化铝也不会溶解,故D错误.
故选C.
A.将氯化铁饱和溶液加入到沸水中可得到氢氧化铁胶体;
B.三价铁离子遇硫氰化钾变红色;
C.铝与碱反应生成偏铝酸钠和氢气;
D.氯化铝与氨水反应生成氢氧化铝白色沉淀,但氢氧化铝不溶于弱碱.

练习册系列答案
相关题目
【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚.其反应原理如下:电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l);电解池:2Al+3H2O ![]() Al2O3+3H2↑,电解过程中,以下判断正确的是( )
Al2O3+3H2↑,电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e﹣=Pb2++2H2O | 阳极:2Al+3H2O﹣6e﹣=Al2O3+6H+ |
D |
|
|
A.A
B.B
C.C
D.D