题目内容
16.下列表示元素的基态原子的电子排布式,其中表示的元素属于第三周期的元素的是( )| A. | 1s22s1 | B. | 1s22s22p5 | ||
| C. | 1s22s22p63s2 | D. | 1s22s22p63s23p64s1 |
分析 元素属于第三周期,则第三周期的元素的最大能层为3,以此来解答.
解答 解:元素属于第三周期的元素,则最大能层为3,所以1s22s1、1s22s22p5、1s22s22p63s23p64s1不是第三周期元素,1s22s22p63s2是属于第三周期的元素,故选C.
点评 本题考查了核外电子排布式与位置的关系,难度较大,掌握判断的方法即可.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
6.下列分子中所有原子未全部满足最外层为8个电子结构的是( )
| A. | N2 | B. | CO2 | C. | BF3 | D. | PCl3 |
7.下列是A、B、C、D、E五种元素的某些性质:
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是D.
A.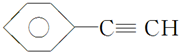 B.CH4
B.CH4
C.CH2═CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键F-H…F、F-H…O、O-H…F、O-H…O.
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是SO2(化学式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
(4)B、D形成的氢化物沸点:H2O更高,热稳定性H2O更强.(写化学式)
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
A.
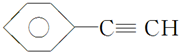 B.CH4
B.CH4C.CH2═CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键F-H…F、F-H…O、O-H…F、O-H…O.
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是SO2(化学式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
(4)B、D形成的氢化物沸点:H2O更高,热稳定性H2O更强.(写化学式)
1.X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是( )
| A. | R一定是共价化合物 | |
| B. | R一定是离子化合物 | |
| C. | R可能是共价化合物,也可能是离子化合物 | |
| D. | R是气态物质 |
8.有关下列图象的分析错误的是( )
| A. | 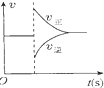 图可表示对平衡N2+3H2?2NH3加压、同时移除部分NH3时的速率变化 | |
| B. | 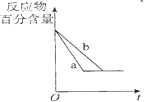 图中a、b曲线只可表示反应H2(g)十I2(g)?2HI(g)在有催化剂和无催化剂存在下建立平衡的过程 | |
| C. | 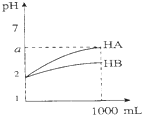 图表示室温下将各1 ml pH=2的HA、HB两种酸溶液加水稀释的情况.若2<a<5,则两酸都为弱酸 | |
| D. | 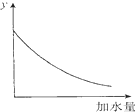 图中的y可表示将O.1 mol/l稀醋酸加水稀释时溶液导电能力的变化情况 |
5.任何科学真理的发现,都不是一帆风顺的,门捷列夫的元素周期表奠定了现代化学和物理学的理论基础.下列关于元素周期表的说法中,不正确的是( )
| A. | 周期表中的副族、Ⅷ族都是金属元素 | |
| B. | 周期表中的ⅡA族都是金属元素 | |
| C. | 周期表中的非金属元素都位于短周期 | |
| D. | 周期表中的0族元素都是非金属元素 |
 、
、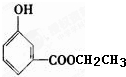 、
、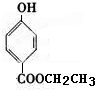 .
.