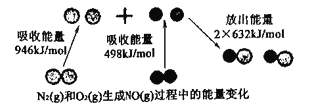
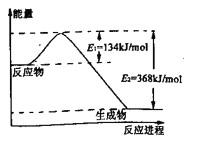
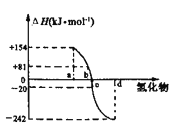
题目内容
【题目】某烷烃和单烯烃的混合气体2.24L,将其完全燃烧,产生的气体缓缓通过浓硫酸,浓硫酸增重4.05克,将剩余气体通入碱石灰,碱石灰质量增加了6.60克,另取该混合气体2.24L通过过量溴水,溴水质量增加了1.05克。
(1)混合气体由哪两种烃组成____?
(2)两种烃的体积分数各是多少______?
【答案】CH4和C3H6 CH4:75%,C3H6:25%
【解析】
根据有机物燃烧时,有机物中的碳全部转化为二氧化碳,其质量可以根据澄清石灰水质量增加量来确定,有机物中的氢全部转化为水,其质量可以根据浓硫酸质量增加来确定,烯烃和溴单质能发生加成反应,溴水质量增加量就是烯烃的质量,根据水以及二氧化碳的量可以确定碳和氢原子的个数之比。
(1)混合气体的物质的量为![]() =0.1mol;燃烧后通过浓H2SO4,增重的质量即水的质量为4.05g,即
=0.1mol;燃烧后通过浓H2SO4,增重的质量即水的质量为4.05g,即![]() =0.225mol,再通过碱石灰,增重的质量即生成CO2的质量为6.60g,即
=0.225mol,再通过碱石灰,增重的质量即生成CO2的质量为6.60g,即![]() =0.15mol;取0.1mol混合物通入溴水,增重的质量即烯烃的质量为1.05g.所以设烷烃、烯烃分别为CxH2x+2、CyH2y,且两种烃的物质的量分别为a,b,则有:1.05g=14yg/mol×b;a+b=0.1mol;(2x+2)a+2yb=0.225mol×2((H守恒);ax+by=0.15mol(C守恒);解得x=1,y=3,a=0.075mol,b=0.025mol,所以烷烃为CH4;
=0.15mol;取0.1mol混合物通入溴水,增重的质量即烯烃的质量为1.05g.所以设烷烃、烯烃分别为CxH2x+2、CyH2y,且两种烃的物质的量分别为a,b,则有:1.05g=14yg/mol×b;a+b=0.1mol;(2x+2)a+2yb=0.225mol×2((H守恒);ax+by=0.15mol(C守恒);解得x=1,y=3,a=0.075mol,b=0.025mol,所以烷烃为CH4;
(2)烯烃为C3H6,CH4的体积分数为![]() ×100%=75%;C3H6的体积分数为
×100%=75%;C3H6的体积分数为![]() ×100%=25%。
×100%=25%。

 字词句段篇系列答案
字词句段篇系列答案【题目】金属蚀刻加工过程中,常用盐酸对其表面氧化物进行清洗,会产生酸洗废水。 pH在1.5左右的某酸洗废水中含铁元素质量分数约3%,其他金属元素如铜、镍、锌、 铬浓度较低,工业上综合利用酸洗废水可制备三氯化铁。制备过程如下:
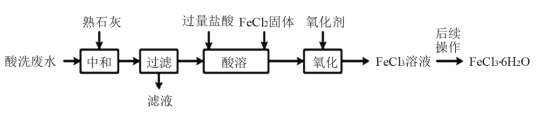
相关金属离子生成氢氧化物沉淀的pH如下表所示:
氢氧化物 | Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 | Cr(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 4.2 | 7.1 | 5.4 | 4.3 | 7.6 |
沉淀完全的pH | 3.7 | 6.7 | 9.2 | 8.0 | 5.6 | 9.6 |
回答下列问题:
(1)“中和”时发生反应的化学方程式为__________________,调节pH至________范围,有利于后续制备得纯度较高的产品。
(2)酸溶处理中和后的滤渣,使铁元素浸出。滤渣和工业盐酸反应时,不同反应温度下 铁浸出率随时间变化如图(a)所示,可知酸溶的最佳温度为_______________。按照不同的固液比(滤渣和工业盐酸的投入体积比)进行反应时,铁浸出率随时间变化如图(b)所示,实际生产中固液比选择1.5:1的原因是___________。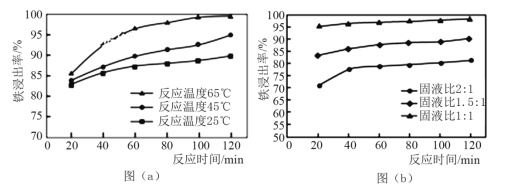
(3)氧化时,可选氯酸钠或过氧化氢为氧化剂,若100L“酸溶”所得溶液中Fe 2+含量为1.2molL1,则需投入的氧化剂过氧化氢的质量为__________。
(4)氧化时,除可外加氧化剂外,也可采用惰性电极电解的方法,此时阴极的电极反应式为__________,电解总反应的离子方程式是 __________。
(5)将得到的FeCl3溶液在HCl气氛中______、______、过滤、洗涤、干燥得FeCl36H2O晶体。