题目内容
【题目】人民网报道,浙江温岭一河流氨氮超标五倍,河水黑如墨水。氮氧化物污染日益严重,请分析下列有关NO、NO2等的试题,然后填空。
(1)下图所示为N2(g)和O2(g)生成NO(g)过程中的能量变化。
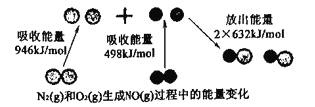
由上图写出N2(g)和O2(g)生成NO(g)的热化学反应方程式____________
(2)下图是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式________________________.
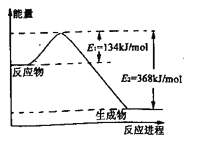
(3)已知:在298K、101kPa下,由稳定的单质生成1mol化合物的反应热叫做该化合物的生成热。如图为氧族元素(除钋外)的氢化物a、b、c、d的生成热数据示意图
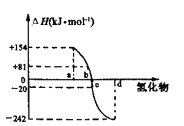
①请归纳:非金属元素的气态氢化物的稳定性与氢化物的生成热(ΔH)之间的关系______________________________
②写出硒化氢在298K、101kPa时发生分解反应的热化学反应方程式__________
【答案】N2(g) + O2(g)=2NO(g)ΔH =+180 kJ/mol NO2(g)+CO(g)=CO2(g)+NO(g)ΔH=-234 kJ/mol 非金属元素的气态氢化物越稳定,ΔH越小,反之亦然 H2Se(g)=H2(g)+Se(s)ΔH=-81 kJ/mol
【解析】
(1)由图:N≡N键的键能为946kJ·mol-1,反应热=反应物总键能-生成物总键能=946kJ·mol-1+498kJ·mol-1-2×632kJ·mol-1=180 kJ·mol-1,热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180 kJ·mol-1;
(2)由图,1mol NO2和1mol CO反应生成CO2和NO放出热量368kJ-134kJ=234kJ,反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ·mol-1;
(3)①非金属元素氢化物的稳定性与生成1mol氢化物时的△H的关系为:根据元素周期律,同一主族元素非金属性越强,生成气态氢化物越容易,气态氢化物越稳定;而根据热力学,能量越低越稳定,a、b、c、d依次为H2Te、H2Se、H2S、H2O,
即:非金属元素氢化物越稳定,△H越小,反之亦然;
由①可知,b为硒化氢的生成热数据,则硒化氢分解放热,且△H=-81kJ·mol-1,所以硒化氢发生分解反应的热化学反应方程式为H2Se(g)=Se(s)+H2(g)△H=-81kJ·mol-1。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案