题目内容
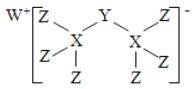
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,W、Z核外电子数之和是X核外电子数的2倍,Y的最外层电子数是其质子数的![]() 。下列叙述正确的是
。下列叙述正确的是
A. X、Z两元素可形成离子化合物
B. 气态氢化物的稳定性:X>Y>Z
C. 该新化合物中的Y元素满足8电子稳定结构
D. Y、Z元素分别对应的最高价氧化物的水化物均是强酸
【答案】C
【解析】
W、X、Y、Z为同一短周期元素,Y的最外层电子数是其质子数的![]() ,Y为Li或P元素,根据化合物的结构示意图,X能形成4个共价键、Z能形成1个共价键,Y能形成2个共价键,则Y只能为P,X位于第IVA族,为Si元素;Z位于第VIIA族,为Cl元素,W、Z核外电子数之和是X核外电子数的2倍, 则W的核外电子数为11,W为Na元素,据此分析解答。
,Y为Li或P元素,根据化合物的结构示意图,X能形成4个共价键、Z能形成1个共价键,Y能形成2个共价键,则Y只能为P,X位于第IVA族,为Si元素;Z位于第VIIA族,为Cl元素,W、Z核外电子数之和是X核外电子数的2倍, 则W的核外电子数为11,W为Na元素,据此分析解答。
根据上述分析可知:W、X、Y、Z分别是Na、Si、P、Cl元素。
A、Si和Cl都是非金属元素,形成共价化合物,故A错误;
B、元素的非金属性越强,气态氢化物越稳定,稳定性:X<Y<Z,故B错误;
C、Y为P元素,其最外层有5个电子,P原子形成2个共价键且该阴离子得到W原子一个电子,所以P原子达到8电子结构,故C正确;
D、磷酸不能完全电离,属于中强酸范畴,不属于强酸,故D错误;
故选C。

 考前必练系列答案
考前必练系列答案【题目】用图表来处理数据是发现科学规律的一种重要方法。
(1)下图是原子序数为1~18的元素原子的最外层电子数随原子序数变化的直方图。图中元素a 是__,b 是____。

(2)下图表示元素的一种性质随原子序数变化的情况,根据分析,该图纵坐标表示的是_________。

(3)下表给出了部分元素的原子半径。
元素符号 | Li | Be | B | C | N | O | F | Na | K | Rb | Cs |
原子半径/nm | 0.152 | 0.089 | 0.082 | 0.077 | 0.075 | 0.074 | 0.071 | 0.186 | 0.227 | 0.248 | 0.265 |
请根据表中数据分析同周期元素原子半径的递变规律是______,同主族元素原子半径的递变规律是_____根据表中得出的规律比较Ca2+和Cl-的半径大小:r(Ca2+)_____r(Cl-)(填“>”“<”或“=”)。