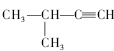
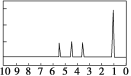
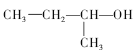��Ŀ����
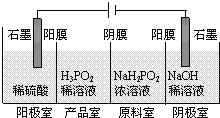
����Ŀ������������ȼ�ϵ�ص���±ˮ(��Cl����Br����Na����Mg2��)��װ����ͼ��ʾ(a��bΪʯī�缫)������˵���У���ȷ����
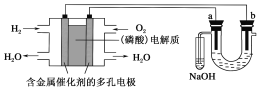
A����ع���ʱ��������ӦʽΪO2��2H2O��4e��===4OH��
B�����ʱ��a�缫��Χ���ȷŵ����Cl����������Br��
C�����ʱ����������·���ǣ������D�����·�D�������D����Һ�D�������D������
D������������ģ������������0.02 g H2ʱ��b����Χ�����0.02 g H2
���𰸡�D
��������
���������A�����Խ����У�����ȼ�ϵ���������������õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪO2+4H++4e���T2H2O��A����B����ԭ��ǿ�������������ȷŵ磬���ʱ��a�缫��Χ���ȷŵ����Br��������Cl�������Ի�ԭ�ԣ�Br����Cl����B������C�����ʱ����������·���ǣ����������·�����������������·��������C����D������ת�Ƶ������֪�������������0.02g H2ʱ��b ����Χ�����0.02g H2��D��ȷ����ѡD��

��ϰ��ϵ�д�
�����Ŀ