��Ŀ����
![]() ����Ŀ����2 L���ܱ������ڣ�800��ʱ��Ӧ2NO(g)��O2(g)
����Ŀ����2 L���ܱ������ڣ�800��ʱ��Ӧ2NO(g)��O2(g)![]()
![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K��_____________________����֪��K300����K350������÷�Ӧ��______�ȷ�Ӧ��
��2����ͼ��ʾNO2�ı仯��������_______����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��_______________��

��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d���������ܶȱ��ֲ���
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________��
a����ʱ�����NO2���� b���ʵ������¶� c������O2��Ũ�� d��ѡ���Ч����
���𰸡���1�� ��
��2��b 1.5��10��3 mol��L��1��s��1 ��3��bc ��4��c
��������
�����������1�����淴Ӧ2NO��g��+O2��g��2NO2��g����ƽ�ⳣ��k=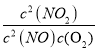 ��K��300�棩��K�� 350������˵�������¶�ƽ�����淴Ӧ�ƶ���������Ӧ�Ƿ��ȷ�Ӧ��
��K��300�棩��K�� 350������˵�������¶�ƽ�����淴Ӧ�ƶ���������Ӧ�Ƿ��ȷ�Ӧ��
��2���ɷ���ʽ2NO��g��+O2��g��2NO2��g����֪��ƽ��ʱ��c��NO������c��O2������c��NO2��=2��1��2���ɱ������ݿ�֪��ƽ��ʱ��c��NO��=![]() =0.00625mol/L������bƽ��ʱ��Ũ��Ϊ0.00625mol/L��������b��ʾNO2��Ũ�ȱ仯��
=0.00625mol/L������bƽ��ʱ��Ũ��Ϊ0.00625mol/L��������b��ʾNO2��Ũ�ȱ仯��![]() ��ͼ�����ݿ�֪2s�ڣ�NO��Ũ�ȱ仯��Ϊ0.01mol/L��0.004mol/L=0.006mol/L����v��NO��=
��ͼ�����ݿ�֪2s�ڣ�NO��Ũ�ȱ仯��Ϊ0.01mol/L��0.004mol/L=0.006mol/L����v��NO��=![]() =0.003mol/��Ls������������֮�ȵ��ڻ�ѧ������֮�ȣ���v��O2��=1/2v��NO��=1/2��0.003mol/��Ls��=1.5��10��3 mol��L��1��s��1 ���ʴ�Ϊ��b��0.0015mol/��Ls������3��a��δָ���������ʣ�����Ϊͬһ�������ʣ�ʼ�ն�����v��NO2��=2v��O2����ϵ���ʲ���˵������ƽ�⣬��Ϊ��ͬ��������ʣ�����֮�ȵ��ڻ�ѧ������֮�ȣ�˵������ƽ�⣬a����
=0.003mol/��Ls������������֮�ȵ��ڻ�ѧ������֮�ȣ���v��O2��=1/2v��NO��=1/2��0.003mol/��Ls��=1.5��10��3 mol��L��1��s��1 ���ʴ�Ϊ��b��0.0015mol/��Ls������3��a��δָ���������ʣ�����Ϊͬһ�������ʣ�ʼ�ն�����v��NO2��=2v��O2����ϵ���ʲ���˵������ƽ�⣬��Ϊ��ͬ��������ʣ�����֮�ȵ��ڻ�ѧ������֮�ȣ�˵������ƽ�⣬a����
b���淴Ӧ�������������ʵ�����С��ѹǿ����С��������ѹǿ���ֲ��䣬˵������ƽ�⣬b��ȷ��c����ͬ���ʱ�ʾ����������֮�ȵ��ڻ�ѧ������֮�ȣ���Ӧ����ƽ�⣬��v����NO��=2v����O2����˵������ƽ�⣬c��ȷ��d����Ӧ���������������䣬����������������ܶ�ʼ�ղ��䣬�����������ʵ��ܶȱ��ֲ��䣬����˵������ƽ�⣬d����ѡbc��
��4��a����ʱ�����NO2���壬ƽ��������Ӧ�ƶ�������Ӧ���ʽ��ͣ�a����b���ʵ������¶ȣ���Ӧ��������ƽ�����淴Ӧ�ƶ���b����c������O2��Ũ�ȣ���Ӧ��������ƽ��������Ӧ�ƶ���c��ȷ��d��ѡ���Ч�Ĵ���������Ӧ���ʣ���Ӱ��ƽ���ƶ���d����ѡc��









