题目内容
15.工业制备氯化铜时,将浓盐酸加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3].请回答以下问题:(1)第一步,如果直接调整pH=9.6,不能将Cu2+和Fe2+分离除去,理由是:Cu2+也被完全沉淀了
现有下列几种常用的氧化剂,可用于氧化除去混合溶液中Fe2+,其中最好选:②.
①KMnO4 ②H2O2 ③NaClO ④浓HNO3
(2)除去溶液中Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有①③.
①Cu(OH)2 ②氨水 ③Cu2(OH)2CO3 ④NaOH
(3)直接加热溶液,蒸干不能(选填“能”或“不能”)得到氯化铜晶体(CuCl2•2H2O).
分析 (1)除去Fe2+时,应避免Cu2+生成沉淀;加入氧化剂时,不能引入新的杂质;
(2)使Fe3+转化为Fe(OH)3沉淀,应调节溶液的pH,所加物质能与酸反应,注意不能引入新杂质;
(3)铜离子水解生成盐酸易挥发,不能得到氯化铜.
解答 解:(1)由题给信息可知,除去Fe2+时,应避免Cu2+生成沉淀,如直接调整溶液pH=9.6,则生成氢氧化亚铁的同时,氢氧化铜、氢氧化铁也同时生成;加入氧化剂时,不能引入新的杂质,如用NaClO,则可引入NaCl杂质,浓硝酸、高锰酸钾的还原产物均引入新杂质,应加入过氧化氢,
故答案为:Cu2+也被完全沉淀了;②;
(2)使Fe3+转化为Fe(OH)3沉淀,应调节溶液的pH,所加物质能与酸反应,注意不能引入新杂质,氨水、NaOH均引入新杂质,则可用CuO 或Cu(OH)2或CuCO3;
故答案为:①③;
(3)加热促进铜离子水解,铜离子水解生成盐酸易挥发,不能得到氯化铜,故答案为:不能.
点评 本题考查较为综合,涉及物质的分离、提纯和制备,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及题给信息,题目难度不大.

练习册系列答案
相关题目
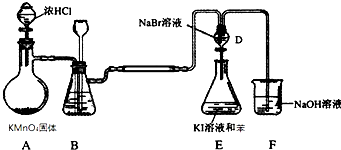
5.如图是氯气的制备以及氯、溴、碘的非金属性比较实验,充分反应一段时间后,打开装置D的活塞,将装置D中少量溶液加入装置E中,振荡,观察实验现象,下列说法正确的是( )

| A. | 装置E下层呈现紫红色 | |
| B. | 装置B中可盛放水吸收氯气中的HCl气体 | |
| C. | F2不能与NaCl溶液反应置换出氯气 | |
| D. | 装置E中有机试剂层呈现紫红色,能说明非金属性Br>I |
6.下列说法不正确的是( )
| A. | 淀粉、纤维素水解的最终产物均为葡萄糖 | |
| B. | 糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应 | |
| C. | 葡萄糖既可以与银氨溶液反应,又可以与新制氢氧化铜悬浊液反应 | |
| D. | 天然油脂没有固定的熔点和沸点,所以天然油脂是混合物 |
10.下列电化学有关说法中正确的是( )
| A. | 将钢闸门与直流电源的正极相连,可降低钢闸门腐蚀速率 | |
| B. | 镀锌铁制品镀层受损后,铁制品仍不易生锈 | |
| C. | 粗铜精炼时,电镀液中的c(Cu2+)保持不变 | |
| D. | 纯银在空气中久置变黑发生的是电化学腐蚀 |
20.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 常温下,1mol Fe与足量稀HNO3反应,转移电子的数目为2NA | |
| B. | 18gD2O中含有的质子数目为10NA | |
| C. | 标准状况下,22.4L二氯甲烷的分子数约为NA | |
| D. | 28g由C2H4和C3H6组成的混合物中含有氢原子的数目为4NA |
7.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 若5.6LN2中含有n个氮分子,则阿伏加德罗常数一定为4n | |
| B. | 4.6gNa与100 mL含0.1mol HCl的盐酸溶液反应,转移电子数目为0.2NA | |
| C. | 14g乙烯和丙烯的混合气体中所含分子总数为0.5NA | |
| D. | 标准状况下,22.4LCCl4含有的分子总数为NA |
2.已知R为ⅡA族元素,L为ⅢA族元素,它们的原子序数分别为m和n,且R、L为同一周期元素,下列关系式错误的是( )
| A. | n=m+1 | B. | n=m+10 | C. | n=m+11 | D. | n=m+25 |