题目内容
3.表是元素同期表的一部分,表中每一序号分别代表一种元素.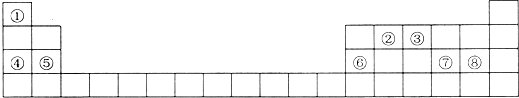
(1)元素③位于第2周期、VA族,该元素属于非金属(填“金属”或“非金属”)元素.
(2)元素④的最高价氧化物对应的水化物的化学式是NaOH.元素②、⑦、⑧的最高价氧化物对应的水化物中,酸性最强的是高氯酸(填物质名称).
(3)表中所列8种元素中,原子半径最小的元素是H(填元素符号).由⑤和⑧两种元素形成的化合物中,含有的化学键是离子键(填“离子键”或“共价键”).
(4)含有元素④的化合物在灼烧时,火焰的颜色为黄色.元素⑤的单质在空气中燃烧时,会发生的现象有放热、产生大量的白烟和发出耀眼的白光.
(5)在元素②、⑥、⑦的最高价氧化物中,能够与水反应生成强酸的氧化物是SO3(填化学式),能够用于制造耐火材料的物质是Al2O3(填化学式).
(6)只含有元素①、③、⑧的一种常见的盐的化学式是NH4Cl.
分析 由元素在周期表中的位置可知,①为H、②为C、③为N、④为Na、⑤为Mg、⑥为Al、⑦为S、⑧为Cl.
(1)元素③位于第2周期VA族,属于非金属性元素;
(2)元素④的最高价氧化物对应的水化物为氢氧化钠,元素非金属性越强,最高价含氧酸的酸性越强;
(3)所有元素中氢原子半径最小;由⑤和⑧两种元素形成的化合物为氯化镁,由镁离子与氯离子构成;
(4)钠元素焰色反应为黄色;镁在空气中燃烧时,会发生的现象有放热、产生大量的白烟和发出耀眼的白光;
(5)在元素②、⑥、⑦的最高价氧化物中,能够与水反应生成强酸的是三氧化硫,能够用于制造耐火材料的物质是氧化铝;
(6)只含有元素H、N、Cl的一种常见的盐为氯化铵.
解答 解:由元素在周期表中的位置可知,①为H、②为C、③为N、④为Na、⑤为Mg、⑥为Al、⑦为S、⑧为Cl.
(1)元素③位于第2周期VA族,属于非金属性元素,故答案为:VA;非金属;
(2)元素④的最高价氧化物对应的水化物为NaOH,非金属性Cl>S>C,故最高价氧化物对应的水化物中,酸性最强的是高氯酸,故答案为:NaOH;高氯酸;
(3)所有元素中氢原子半径最小;由⑤和⑧两种元素形成的化合物为氯化镁,由镁离子与氯离子构成,含有离子键,故答案为:H;离子键;
(4)④为Na,其化合物灼烧时,火焰为黄色;镁在空气中燃烧时,会发生的现象有放热、产生大量的白烟和发出耀眼的白光,故答案为:黄色;发出耀眼的白光;
(5)在元素②、⑥、⑦的最高价氧化物分别为二氧化碳、氧化铝、三氧化硫,能够与水反应生成强酸的是SO3,能够用于制造耐火材料的物质是Al2O3,故答案为:SO3;Al2O3;
(6)只含有元素H、N、Cl的一种常见的盐为NH4Cl,故答案为:NH4Cl.
点评 本题考查元素周期表与元素周期律,比较基础,注意对基础知识的掌握.

 口算能手系列答案
口算能手系列答案| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 分子中可能含有氧原子 | D. | 有机物的分子式为CH4Ox(x=O、1) |
| A. | 存在于氧气和三氧化硫中 | B. | 只存在于三氧化硫中 | ||
| C. | 三种物质中都有 | D. | 无法判断 |
( )
| A. | 乙烷 | B. | 苯 | C. | 乙烯 | D. | 乙醇 |
| A. | 元素的相对原子质量 | B. | 原子的核内中子数 | ||
| C. | 原子的次外层电子数 | D. | 原子的电子层数和最外层电子数 |
| A. | 化学平衡常数反映了在一定温度下可逆反应可能进行的限度 | |
| B. | 四种平衡常数都是温度的函数,温度升高其数值都增大 | |
| C. | 一个可逆反应的化学平衡常数和参与反应的每种物质的化学计量数都有关系 | |
| D. | 纯水中加入强酸或强碱,水的离子积常数都会减小 |
| A. | 31g白磷中含有的共价键数目为1.5NA | |
| B. | 0.1L3.0mol•L-1的NH4N03溶液中含有的NH4+的数目为0.3NA | |
| C. | 标准状况下,22.4L己烷中含共价键数目为19NA | |
| D. | 常温常压下,lmolCl2与足量的水充分反应,转移的电子数目为NA |
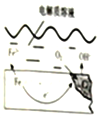 如图是钢铁在潮湿空气能发生电化学腐蚀原理示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈
如图是钢铁在潮湿空气能发生电化学腐蚀原理示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈