题目内容
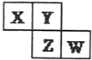
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若X与Z的质子数之和为23。下列说法正确的是
A. X气态氢化物的水溶液呈酸性 B. 氧化物对应水化物的酸性:W>Z>X
C. Z、W简单离子半径Z>W D. W的单质具有漂白性,Z的氧化物不具有漂白性
【答案】C
【解析】X、Y、Z、W均为短周期元素,依据其所在表格中的相对位置知X、Y位于第二周期,Z、W位于第三周期,且X与Z的质子数之和为23,设X的质子数为a,则Y为a+1,Y为a+9,W为a+10,即a+(a+9)=23,解得:a=7,据此得出X为N,Y为O,Z为S,Z为S、W为Cl,据此判断各选项即可。
根据以上分析可知X为N,Y为O,Z为S、W为Cl,则
A.氮元素的氢化物氨气是碱性气体,其水溶液显碱性,A错误;
B.非金属性越强,最高价氧化物水化物的酸性越强,其它含氧酸则不一定,B错误;
C.离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则Z、W简单离子半径Z>W,C正确;
D.氯气不具有漂白性,溶于水生成的次氯酸具有漂白性,Z的氧化物二氧化硫具有漂白性,D错误;
答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素③的原子结构示意图______;元素⑨形成的氢化物的电子式___________。
(3)表中元素④、⑨形成的氢化物的稳定性顺序为_____> (填化学式)。
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为_____> (填化学式)。
(5)表中元素③、④、⑥、⑦的原子半径大小为____> > > (填元素符号)。
【题目】已知常温下浓度为0.lmol/L的下列溶液的pH如下表,下列有关说法正确的是
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序: H2CO3<HClO<HF
B. 根据上表,水解方程式ClO-+H2O![]() HClO+OH-的水解常数K=10-7.6
HClO+OH-的水解常数K=10-7.6
C. 若将CO2通入0.lmol/LNa2C03溶液中至溶液中性,则溶液中2c(CO32-)+c(HCO3-)=0.1 mol/L
D. 向上述NaC1O溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>(H+)>c(HClO)>c(OH-)