ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩœ¬±μΈΣ‘ΣΥΊ÷ήΤΎ±μΒΡ“Μ≤ΩΖ÷Θ§«κΑ¥“Σ«σΜΊ¥πΈ ΧβΘΚ
Ήε ÷ήΤΎ | ΔώA | ΔρA | ΔσA | ΔτA | ΔθA | ΔωA | ΔςA | 0 |
2 | ΔΌ | ΔΎ | Δέ | Δή | Δί | |||
3 | Δό | ΔΏ | Δύ | Δα |
Θ®1Θ©±μ÷–‘ΣΥΊ______ΒΡΖ«Ϋπ τ–‘Ήν«ΩΘ§‘ΣΥΊ_____ΒΡΫπ τ–‘Ήν«ΩΘ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
Θ®2Θ©±μ÷–‘ΣΥΊΔέΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦ______ΘΜ‘ΣΥΊΔα–Έ≥…ΒΡ«βΜ·ΈοΒΡΒγΉ” Ϋ___________ΓΘ
Θ®3Θ©±μ÷–‘ΣΥΊΔήΓΔΔα–Έ≥…ΒΡ«βΜ·ΈοΒΡΈ»Ε®–‘Υ≥–ρΈΣ_____ΘΨΓΓ ΓΓΘ®ΧνΜ·―ß ΫΘ©ΓΘ
Θ®4Θ©±μ÷–‘ΣΥΊΔύΚΆΔαΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘«Ω»θΈΣ_____ΘΨΓΓ ΓΓΘ®ΧνΜ·―ß ΫΘ©ΓΘ
Θ®5Θ©±μ÷–‘ΣΥΊΔέΓΔΔήΓΔΔόΓΔΔΏΒΡ‘≠Ή”ΑκΨΕ¥σ–ΓΈΣ____ΘΨΓΓ ΓΓΘΨΓΓ ΓΓΘΨΓΓ Θ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
ΓΨ¥πΑΗΓΩ F Na ![]()
![]() HFΓΓ ΓΓHCl HClO4ΓΓΓΓH2SO4 NaΓΓΓΓMgΓΓΓΓOΓΓΓΓF
HFΓΓ ΓΓHCl HClO4ΓΓΓΓH2SO4 NaΓΓΓΓMgΓΓΓΓOΓΓΓΓF
ΓΨΫβΈωΓΩ”…‘ΣΥΊ‘Ύ÷ήΤΎ±μΒΡΈΜ÷ΟΩ…“‘÷ΣΒά,ΔΌ~ΔαΖ÷±πΈΣLiΓΔCΓΔOΓΔFΓΔNeΓΔNaΓΔMgΓΔSΓΔClΘ§
(1)ΕΧ÷ήΤΎ÷°÷–FΒΡΖ«Ϋπ τ–‘Ήν«ΩΘ§NaΒΡΫπ τ–‘Ήν«ΩΘΜ(2)OΒΡ‘≠Ή”–ρ ΐΈΣ8Θ§Δα–Έ≥…ΒΡ«βΜ·ΈοΈΣHClΘΜ(3)Ζ«Ϋπ τ–‘‘Ϋ«ΩΘ§Ε‘”Π«βΜ·Έο‘ΫΈ»Ε®ΘΜ(4)Ζ«Ϋπ τ–‘‘Ϋ«ΩΘ§Ε‘”ΠΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘‘Ϋ«ΩΘΜ(5)ΒγΉ”≤ψ‘ΫΕύΘ§‘≠Ή”ΑκΨΕ‘Ϋ¥σΘ§Ά§÷ήΤΎ¥”Ήσœρ”“‘≠Ή”ΑκΨΕΦθ–ΓΓΘ
”…‘ΣΥΊ‘Ύ÷ήΤΎ±μΒΡΈΜ÷ΟΩ…“‘÷ΣΒά,ΔΌ~ΔαΖ÷±πΈΣLiΓΔCΓΔOΓΔFΓΔNeΓΔNaΓΔMgΓΔSΓΔClΘ§
(1)±μ÷–‘ΣΥΊFΒΡΖ«Ϋπ τ–‘Ήν«Ω,‘ΣΥΊNaΒΡΫπ τ–‘Ήν«Ω,“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «:F;Na;
(2)OΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦΈΣ![]() ΘΜ‘ΣΥΊΔα–Έ≥…ΒΡ«βΜ·ΈοΈΣHClΘ§ΤδΒγΉ” ΫΈΣ
ΘΜ‘ΣΥΊΔα–Έ≥…ΒΡ«βΜ·ΈοΈΣHClΘ§ΤδΒγΉ” ΫΈΣ![]() Θ§“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «ΘΚ
Θ§“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «ΘΚ![]() ΘΜ
ΘΜ![]() ΘΜ
ΘΜ
(3)±μ÷–‘ΣΥΊΔήΓΔΔα–Έ≥…ΒΡ«βΜ·ΈοΒΡΈ»Ε®–‘Υ≥–ρΈΣHF>HClΘ§“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «:HFΘΜHClΘΜ
(4)±μ÷–‘ΣΥΊΔύΚΆΔαΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘«Ω»θΈΣHClO4>H2SO4Θ§“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «: HClO4ΘΜH2SO4ΘΜ
(5)±μ÷–‘ΣΥΊΔέΓΔΔήΓΔΔόΓΔΔΏΒΡ‘≠Ή”ΑκΨΕ¥σ–ΓΈΣNa>Mg>O>FΘ§“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «:NaΘΜMgΘΜOΘΜFΓΘ

 –Γ―ßΩΈ ±ΧΊ―ΒœΒΝ–¥πΑΗ
–Γ―ßΩΈ ±ΧΊ―ΒœΒΝ–¥πΑΗΓΨΧβΡΩΓΩœ¬Ν–ΡΡ“ΜΉι‘ΣΥΊΒΡ‘≠Ή”ΦδΖ¥”Π»ί“Ή–Έ≥…άκΉ”Φϋ( )
‘≠Ή” | a | b | c | d | e | f | g |
M≤ψΒγΉ” ΐ | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
A.aΚΆcB.dΚΆfC.dΚΆgD.bΚΆg
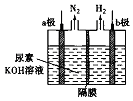
ΓΨΧβΡΩΓΩΝΣή–Θ® ![]() Θ© «“Μ÷÷÷Ί“ΣΒΡ”–ΜζΚœ≥…÷–ΦδΧεΘ§ Β―ι “Ω…”Ο±ΫΚΆ1Θ§2“ΜΕ଻““ΆιΘ®ClCH2CH2ClΘ©ΈΣ‘≠ΝœΘ§‘ΎΈόΥ°AlCl3¥ΏΜ·œ¬Φ”»»÷ΤΒΟΘ§Τδ÷Τ»Γ≤Ϋ÷ηΈΣΘΚ
Θ© «“Μ÷÷÷Ί“ΣΒΡ”–ΜζΚœ≥…÷–ΦδΧεΘ§ Β―ι “Ω…”Ο±ΫΚΆ1Θ§2“ΜΕ଻““ΆιΘ®ClCH2CH2ClΘ©ΈΣ‘≠ΝœΘ§‘ΎΈόΥ°AlCl3¥ΏΜ·œ¬Φ”»»÷ΤΒΟΘ§Τδ÷Τ»Γ≤Ϋ÷ηΈΣΘΚ
Θ®1Θ©¥ΏΜ·ΦΝΒΡ÷Τ±ΗΘΚΆΦ1 « Β―ι “÷Τ»Γ…ΌΝΩΈόΥ°AlCl3ΒΡœύΙΊ Β―ιΉΑ÷ΟΒΡ“«ΤςΚΆ“©ΤΖΘΚ 
ΔΌΫΪ…œ ω“«ΤςΝ§Ϋ”≥…“ΜΧΉ÷Τ±Η≤Δ±Θ¥φΈόΥ°AlCl3ΒΡΉΑ÷ΟΘ§ΗςΙήΩΎ±ξΚ≈Ν§Ϋ”Υ≥–ρΈΣΘΚdΫ”eΘ§Ϋ” Θ§ Ϋ” Θ§ Ϋ” Θ°
ΔΎ”–»ΥΫ®“ιΫΪ…œ ωΉΑ÷Ο÷–D»ΞΒτΘ§Τδ”ύΉΑ÷ΟΚΆ ‘ΦΝ≤Μ±δΘ§“≤Ρή÷Τ±ΗΈόΥ°AlCl3 Θ° Ρψ»œΈΣ’β―υΉω «ΖώΩ…––Θ®ΧνΓΑΩ…––Γ±ΜρΓΑ≤ΜΩ…––Γ±Θ©Θ§ΡψΒΡάμ”… « Θ°
ΔέΉΑ÷ΟA÷–“ΰ≤ΊΉ≈“Μ÷÷Α≤»Ϊ“ΰΜΦΘ§«κΧα≥ω“Μ÷÷ΗΡΫχΖΫΑΗΘΚ Θ°
Θ®2Θ©ΝΣή–ΒΡ÷Τ±Η ΝΣή–ΒΡ÷Τ»Γ‘≠άμΈΣΘΚ ![]()
Ζ¥”ΠΉνΦ―ΧθΦΰΈΣnΘ®±ΫΘ©ΘΚnΘ®1Θ§2©¹Ε଻““ΆιΘ©=10ΘΚ1Θ§Ζ¥”ΠΈ¬Ε»‘Ύ60©¹65Γφ÷°ΦδΘ° Β―ι “÷Τ»ΓΝΣή–ΒΡΉΑ÷Ο»γΆΦ2Υυ ΨΘ®Φ”»»ΚΆΦ”≥÷“«Τς¬‘»ΞΘ©ΘΚ
Β―ι≤Ϋ÷ηΘΚ
‘Ύ»ΐΩΎ…’ΤΩ÷–Φ”»κ120.0mL±ΫΚΆ ΝΩΈόΥ°AlCl3 Θ§ ”…ΒΈ“Κ¬©ΕΖΒΈΦ”10.7mL1Θ§2©¹Ε଻““ΆιΘ§ΩΊ÷ΤΖ¥”ΠΈ¬Ε»‘Ύ60©¹65ΓφΘ§Ζ¥”Π‘Φ60minΘ°ΫΪΖ¥”ΠΚσΒΡΜλΚœΈο“ά¥Έ”ΟœΓ―ΈΥαΓΔ2%Na2CO3»ή“ΚΚΆH2Oœ¥Β”Ζ÷άκΘ§‘ΎΥυΒΟ≤ζΈο÷–Φ”»κ…ΌΝΩΈόΥ°MgSO4ΙΧΧεΘ§Ψ≤÷ΙΓΔΙΐ¬ΥΘ§œ»≥Θ―Ι’τΝσΘ§‘ΌΦθ―Ι’τΝσ ’Φ·170ΓΪ172ΓφΒΡΝσΖ÷Θ§ΒΟΝΣή–18.2gΘ°
œύΙΊΈοάμ≥Θ ΐΚΆΈοάμ–‘÷ »γœ¬±μ
Οϊ≥Τ | œύΕ‘Ζ÷Ή”÷ ΝΩ | ΟήΕ»/Θ®gcm©¹3Θ© | »έΒψ/Γφ | Ζ–Βψ/Γφ | »ήΫβ–‘ |
±Ϋ | 78 | 0.88 | 5.5 | 80.1 | Ρ―»ήΥ°Θ§“Ή»ή““¥Φ |
1Θ§2“ΜΕ଻““Άι | 99 | 1.27 | ©¹35.3 | 83.5 | Ρ―»ήΥ°Θ§Ω…»ή±Ϋ |
ΈόΥ°¬»Μ·¬Ν | 133.5 | 2.44 | 190 | 178Θ®…ΐΜΣΘ© | ”ωΥ°Υ°ΫβΘ§ΈΔ»ή±Ϋ |
ΝΣή– | 182 | 0.98 | 52 | 284 | Ρ―»ήΥ°Θ§“Ή»ή±Ϋ |
Δή“«ΤςaΒΡΟϊ≥ΤΈΣ Θ§ ΚΆΤ’Ά®Ζ÷“Κ¬©ΕΖœύ±»Θ§ Ι”ΟΒΈ“Κ¬©ΕΖΒΡ”≈Βψ « Θ°
Δίœ¥Β”≤ΌΉς÷–Θ§Υ°œ¥ΒΡΡΩΒΡ «ΘΜΈόΥ°ΝρΥαΟΨΒΡΉς”Ο « Θ°
Δό≥Θ―Ι’τΝσ ±Θ§ΉνΒΆΩΊ÷ΤΈ¬Ε» « Θ°
ΔΏΗΟ Β―ιΒΡ≤ζ¬ ‘ΦΈΣ Θ° Θ®–Γ ΐΒψΚσ±ΘΝτΝΫΈΜ”––ß ΐΉ÷Θ©