��Ŀ����
����Fe2+��I-��Br-����Һ��ͨ��������������Һ�и������ӵ����ʵ����仯����ͼ��ʾ���й�˵������ȷ����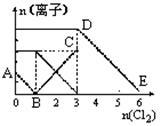
| A���߶�BC����Fe3+���ʵ����ı仯��� |
| B��ԭ�����Һ��n(FeBr2)��3mol |
| C����ͨ��Cl22molʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ�� 2Fe2++2I-+2C12��2Fe3++I2+4Cl- |
| D��ԭ��Һ��n(Fe2+):n(I-):n(Br-)��3:1: 2 |
D
�������������Fe2+��I-��Br-�Ļ�ԭ��ǿ��˳��ΪI->Fe2+>Br,AB��ʾI-�����ʵ����ı仯������ʽΪ2I-+C12��I2+2Cl-��n(I-)=2mol���߶�BC����Fe3+���ʵ����ı仯������ʽΪ2Fe2++C12��2Fe3+ +2Cl-��n(Fe2+)=4mol��DE�α�ʾBr-�����ʵ����ı仯�������ӦΪ2Br-+C12��Br2+2Cl-��n(Br-)=6mol��ԭ��Һ��n(Fe2+):n(I-):n(Br-)��1:2:3,D����
���㣺��������ԭ��Ӧ��صļ��㡣

����ʵ��������������ԭ��Ӧ�йص���
| A��SO2ͨ��Ʒ����Һ�У���Һ��ɫ |
| B��������ˮ�ܱշ���һ��ʱ���dz����ɫ��ʧ |
| C����Fe2(SO4)3��Һ�еμ�NaOH��Һ�����ɺ��ɫ���� |
| D�����������Һ�еμ�������ϡ���ᣬ�����������γ� |
Ϊ�˲ⶨijͭ���Ͻ�ɷ֣���30 g�Ͻ���ȫ����80 mL 13.5 mol/L��Ũ�����У�����Ӧ��ȫ���ռ���0.3 mol���壬�������Һ��c(H+)��1 mol/L�����跴Ӧ����Һ�����Ϊ80 mL����Ͻ���������������Ϊ
| A��36% | B��66.3% | C��78.7% | D��96.6% |
������ѧ������ܻ�ù�����߿�ѧ���������Ա�������ϡ����ȡ���۷��������Ĺ��ס���֪�������棨ϡ��Ԫ�أ��ڿ������������䰵������ʱȼ�գ���ˮ�ܿ췴Ӧ����ע���泣���Ļ��ϼ�Ϊ+3��+4�������ԣ�Ce4+>Fe3+>I2��������˵����ȷ����
A�������������Ļ�ѧ����ʽ�ɱ�ʾΪ��Ce + 4HI  CeI4 + 2H2�� CeI4 + 2H2�� |
| B����Ce(SO4)2��Һ�ζ�����������Һ�������ӷ���ʽΪ��Ce4+ + 2Fe2+ = Ce3+ + 2Fe3+ |
| C����һ�������£��������״̬��CeO2��Ce������������� |
| D��������ֺ���13658Ce��13858Ce��14058Ce��14258Ce�����ǻ���Ϊͬ�������� |
���������У���ȷ����
| A��ֻ���н���Ԫ�ص����Ӳ�һ���������� |
| B�����������ӱ���ԭ��һ���õ��������� |
| C��������ԭ��Ӧ�У��ǽ������ʱ��������� |
| D��Ԫ�شӻ���̬��Ϊ����̬ʱ��һ������ԭ |
�������ײ�����ȱλ�����Σ�MFe2Ox��3<x<4��M��Mn��Co��Zn��Ni���ڸ����о��ԣ�2�ۣ��������Σ�MFe2O4����������������Ӧ�Ƶã������£�����ʹ��ҵ�����е����������SO2��NO2�ȣ�ת��Ϊ�䵥�ʳ�ȥ��ת��������ͼ�����ڴ�ת�����̵���������ȷ����
| A��MFe2O4����H2�ķ�Ӧ�б����������� |
| B��MFe2O4��MFe2Ox���ת����Ӧ������������ԭ��Ӧ |
| C��MFe2Ox��SO2��Ӧ��MFe2Ox����ԭ |
| D����4 mol MFe2Ox��1 mol SO2ǡ����ȫ��Ӧ����MFe2Ox��x��ֵΪ3��5 |
����������ȷ����
��7Li+�к��е��������������֮��Ϊ2��1
����C2H6�����м��Թ��ۼ���Ǽ��Թ��ۼ���֮��Ϊ3��1
�۳����£�11.2 L�ļ��������к��е��⡢̼ԭ����֮��Ϊ4��1
��5.6 g����������������Ӧʧȥ�ĵ�������뷴Ӧ���������ʵ���֮��Ϊ2��1
| A���٢� | B���ڢ� | C���٢� | D���ۢ� |
��֪������ԭ��Ӧ��2Cu(IO3)2��24KI��12H2SO4��2CuI����13I2��12K2SO4��12H2O������1mol�������ڷ�Ӧ�еõ��ĵ���Ϊ
| A��10mol | B��11mol | C��12mol | D��13mol |
���ݱ�����Ϣ�жϣ�����ѡ���ȷ����
| ��� | ��Ӧ�� | ���� |
| �� | KMnO4 ��H2O2 ��H2SO4 | K2SO4 ��MnSO4 ������������ |
| �� | Cl2 ��FeBr2 | FeCl3��FeBr3 |
| �� | MnO4�������������� | Cl2 ��Mn2+ ������������ |
A���ڢ��鷴Ӧ���������ΪH2O�� O2
B���ڢ��鷴Ӧ��Cl2 �� FeBr2�����ʵ���֮��С�ڻ����1�U2
C���ڢ��鷴Ӧ������1mol Cl2��ת�Ƶ���2mol
D����������ǿ����˳��ΪMnO4- > Cl2 > Fe3+ > Br2