题目内容
【题目】水煤气法制取甲醇(CH3OH)的反应及其反应的焓变、平衡常数如下:
① CH4(g) +1/2O2(g)![]() CO(g) + 2H2(g) △H1 =-35.4kJ·mol-1 平衡常数K1
CO(g) + 2H2(g) △H1 =-35.4kJ·mol-1 平衡常数K1
② CO(g) + 2H2(g) ![]() CH3OH (g) △H2 =-90.1 kJ·mol-1 平衡常数K2
CH3OH (g) △H2 =-90.1 kJ·mol-1 平衡常数K2
③ 2CH4(g) + O2(g) ![]() 2CH3OH(g) △H3 平衡常数K3
2CH3OH(g) △H3 平衡常数K3
(1)在25℃、101kPa下,1g液态甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________________________。
(2)依据盖斯定律求出反应③ 2CH4(g) + O2(g) ![]() 2CH3OH(g) △H3 =_____kJ·mol-1,相同温度下K3=______(用含K1、K2代数式表示)。
2CH3OH(g) △H3 =_____kJ·mol-1,相同温度下K3=______(用含K1、K2代数式表示)。
(3)下列关于化学反应中的能量及变化理解错误的是(填字母序号)______。
a.反应中活化能的作用是使反应物活化,从而启动反应或改变反应速率
b.化学键的断裂与形成一定伴随着电子的转移和能量变化
c.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差即焓变(△H)决定
d.氯化钠晶体熔化时,离子键被破坏,吸收能量,发生化学变化
e.200℃、101kPa时,1 mol H2和碘蒸气作用生成HI的反应,热化学方程式表示如下:H2(g)+I2(g) === 2HI(g) △H= -14.9 kJ·mol-1
f.燃烧热定义中“生成稳定的氧化物”,意味着这些氧化物不能再燃烧了
【答案】CH3OH(l)+3/2O2(g)=CO 2(g)+2H2O(l) ΔH=-725.76kJ·mol-1 -251 K12·K22 b d e
【解析】
(1)由1g液态甲醇燃烧放热22.68kJ,则1mol CH3OH燃烧放热22.68 kJ×32=725.76kJ,并在热化学方程式中标明物质的状态;
(2)根据盖斯定律求反应热;通过化学方程式加和求反应的平衡常数;
(3)a.活化能的作用在于使反应物活化,从而启动反应或改变反应速率;
b.成键释放能量,但不一定发生氧化还原反应;
c.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差即焓变(△H)决定;
d.氯化钠熔化只有离子键的断裂,没有新键的形成,不属于化学变化;
e.没有反应热数据,不能写出热化学方程式;
f. “生成稳定的氧化物” 指在燃烧的过程中不会再发生反应的氧化物,也就是完全燃烧。
(1) 由1g液态甲醇燃烧放热22.68kJ,则1mol CH3OH燃烧放热22.68 kJ×32=725.76kJ,则该燃烧反应的热化学方程式为CH3OH(l)+3/2O2(g)=CO 2(g)+2H2O(l) ΔH=-725.76kJ·mol-1,
因此,本题正确答案是:CH3OH(l)+3/2O2(g)=CO 2(g)+2H2O(l) ΔH=-725.76kJ·mol-1;
(2)已知:① CH4(g) +1/2O2(g)![]() CO(g) + 2H2(g) △H1 =-35.4kJ·mol-1
CO(g) + 2H2(g) △H1 =-35.4kJ·mol-1
② CO(g) + 2H2(g) ![]() CH3OH (g) △H2 =-90.1 kJ·mol-1
CH3OH (g) △H2 =-90.1 kJ·mol-1
根据盖斯定律,①×2+②×2得③ 2CH4(g) + O2(g) ![]() 2CH3OH(g)
2CH3OH(g)
故△H3 =(-35.4kJ·mol-1)×2+(-90.1 kJ·mol-1 )×2=-251kJ·mol-1,
相同温度下K3=![]() =
=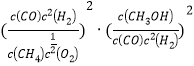 = K12·K22,
= K12·K22,
因此,本题正确答案是:-251 ;K12·K22 ;
(3)a.活化能的作用在于使反应物活化,从而启动反应或改变反应速率,故a正确;
b.成键释放能量,但不一定发生氧化还原反应,则化学键的形成一定伴随着能量变化,不一定存在电子的转移,故b错误;
c.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差即焓变(△H)决定,故c正确;
d.化学变化是旧键的断裂和新键的形成,氯化钠熔化只有离子键的断裂,没有新键的形成,不属于化学变化,故d错误;
e.没有反应热数据,不能写出热化学方程式,故e错误;
f. “生成稳定的氧化物” 指在燃烧的过程中不会再发生反应的氧化物,也就是完全燃烧,故f正确。
因此,本题答案选:b d e。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案