题目内容
【题目】下图是研究铁钉腐蚀的装置图,下列说法不正确的是
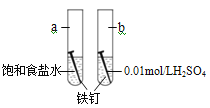
A. 铁钉在两处的腐蚀速率:a < b
B. a、b两处铁钉中碳均正极
C. a、b两处铁钉中的铁均失电子被氧化
D. a、b两处的正极反应式均为O2+4e-+4H+===2H2O
【答案】D
【解析】
试题a中电解质溶液显中性,为铁钉的吸氧腐蚀,b中电解质溶液为稀硫酸,显酸性为析氢腐蚀;
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢;
B、a、b中C为原电池的正极;
C、a、b中Fe失电子为原电池的负极;
D、a中正极上氧气的得电子,b中正极上氢离子得电子.
解:a中电解质溶液显中性,为铁钉的吸氧腐蚀,b中电解质溶液为稀硫酸,显酸性为析氢腐蚀;
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢,所以ab在两处的腐蚀速率a<b,故A正确;
B、a中C为原电池的正极,正极上氧气得电子,b中C为原电池的正极,正极上氢离子得电子,故B正确;
C、原电池中失电子的一极为负极,a、b中Fe失电子为原电池的负极,故C正确;
D、a中正极上氧气得电子,其电极反应式为O2+4e﹣+2H2O═4OH﹣,b中正极上氢离子得电子,其电极反应式为2H++2e﹣=H2↑,故D错误;
故选D.

练习册系列答案
相关题目





