题目内容
16.“低碳”既是时尚,也是环保要求.“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂今后联合生产等都是很好的“低碳”生产方式.下面是几个工厂利用废气、废渣(液)联合生产化肥硫酸铵的工艺:
请回答下列问题:
(1)工艺操作②为:过滤.
(2)工业合成氨的化学方程式为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
(3)副产品的化学式为CaO.该联合生产工艺中可以循环使用的物质是CO2.
(4)在实验室中检验合成氨厂排出的废气中是否含有氨气的方法是用湿润的红色石蕊试纸放在导气管口,若试纸变蓝,则证明有NH3
(5)写出生成“产品”的化学方程式:CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4.
分析 (1)根据反应原理CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4判断操作方法;
(2)工业上用氮气和氢气在高温 高压、催化剂条件下反应生成氨气,据此写出反应的化学方程式;
(3)煅烧碳酸钙后可生成CO2和CaO,其中CO2可循环使用;
(4)通常利用湿润的红色石蕊试纸检验NH3;
(5)“产品”为(NH4)2SO4,反应物为CaSO4悬浊液、CO2、NH3等,产物除(NH4)2SO4外还有CaCO3,据此写出反应的化学方程式.
解答 解:(1)该反应原理为:CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4,将沉淀池中的混合物经过滤可得到产品和沉淀,
故答案为:过滤;
(2)工业上用氮气和氢气在高温 高压、催化剂条件下反应生成氨气,反应的化学方程式为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,
故答案为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3;
(3)CaCO3煅烧后可生成CO2和CaO,其中CO2可循环使用,
故答案为:CaO;CO2;
(4)利用湿润的红色石蕊试纸检验NH3,操作方法为:用湿润的红色石蕊试纸放在导气管口,若试纸变蓝,则证明有NH3,
故答案为:用湿润的红色石蕊试纸放在导气管口,若试纸变蓝,则证明有NH3;
(5)“产品”是(NH4)2SO4,反应物是CaSO4悬浊液、CO2、NH3等,产物除(NH4)2SO4外还有CaCO3,反应化学方程式为CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4,
故答案为:CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4.
点评 本题考查了物质制备方法,题目难度中等,明确制备流程及发生反应原理为解答关键,注意掌握化学实验基本操作方法,试题侧重考查学生的分析能力及化学实验能力.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案(1)100mL 0.2mol/LAl2(SO4)3溶液中含SO42-0.06 mol,含Al3+的物质的量浓度0.4mol•L
(2)3mol O2与2mol O3质量之比为1:1,它们在同温同压下的体积比是3:2
(3)标准状况下,22.4mL氨气溶于水,配成1000mL溶液,问所得溶液的物质的量浓度0.001mol•L
(4)5.6g 硅单质与NaOH完全反应,问转移电子数为0.8mol
(5)要除去下列物质中少量杂质(括号内是杂质),应采取什么方法?写出有关反应的离子方程式:
| 物质 | 所加试剂(填化学式) | 离子方程式 |
| ①Mg(OH)2(Al(OH)3) | ||
| ②NaHCO3溶液(Na2CO3) | ||
| ③FeCl2溶液(FeCl3) |
| 阳离子 | Ag+、Na+ |
| 阴离子 | NO3-、SO42-、Cl- |
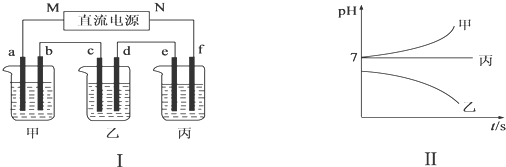
(1)M为电源的负(填“正”或“负”)极,乙中阳离子向c(填“c”或“d”)定向移动,A是NaCl(填写化学式).
(2)计算电极f上生成的气体在标准状况下的体积为1.4L.
(3)b电极上发生的电极反应为2Cl--2e-=Cl2↑;乙烧杯的电解池总反应的化学方程式为4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3.
(4)要使丙恢复到原来的状态,应加入物质的质量为2.25g.
| A. | 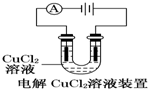 装置中阴极产生的气体能够使湿润淀粉KI试纸变蓝 | |
| B. | 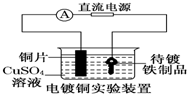 装置中待镀铁制品应与电源正极相连 | |
| C. |  装置中电子由b极流向a极 | |
| D. |  装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
| A. | 原子半径:丁>丙>乙 | |
| B. | 甲的气态氢化物的水溶液呈酸性 | |
| C. | 乙与丙形成的化合物既能与酸反应,又能与碱反应 | |
| D. | 同周期元素中丁的最高价氧化物对应水化物的酸性最强 |
| A. | 两种气体被完全吸收,并生成BaSO4沉淀 | |
| B. | 两种气体被完全吸收,生成BaSO3和BaSO4沉淀 | |
| C. | 两种气体均不能被吸收,没有沉淀生成 | |
| D. | 只有一种气体被吸收,生成BaSO4沉淀 |
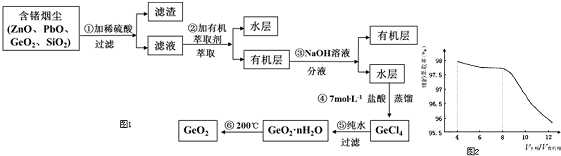
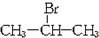 ,且烃A的结构简式为
,且烃A的结构简式为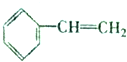 ,其在不同条件下能发生下图所示的一系列变化.
,其在不同条件下能发生下图所示的一系列变化.
 ,D
,D ,E
,E ,H
,H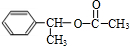 .
. +NaBr.
+NaBr. .
.