题目内容
【题目】下列关于各图的叙述正确的是( )
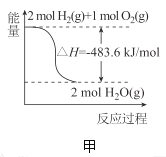
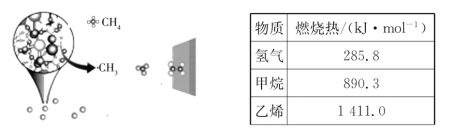
A.甲表示![]() 与
与![]() 发生反应过程中的能量变化,则
发生反应过程中的能量变化,则![]() 的燃烧热为
的燃烧热为![]()
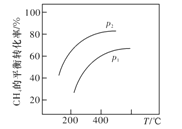
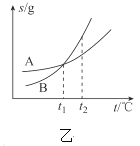
B.乙表示A、B两物质的溶解度随温度变化情况,将![]() 时A、B的饱和溶液分别升温至
时A、B的饱和溶液分别升温至![]() 时,溶质的质量分数
时,溶质的质量分数![]()
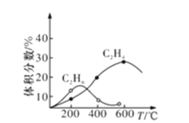
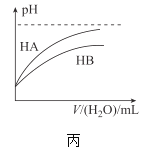
C.丙表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同浓度的NaA溶液的pH小于同浓度NaB溶液的pH
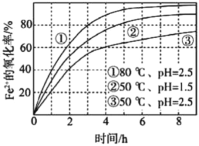
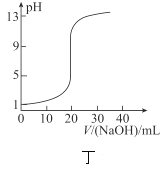
D.丁表示![]() 溶液滴定
溶液滴定![]() 醋酸溶液得到的滴定曲线
醋酸溶液得到的滴定曲线
【答案】C
【解析】
A、燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,图中燃烧产物不是稳定氧化物,所以不是燃烧热,选项A错误;
B、t1℃时A、B溶质质量分数相同,升温时溶液都变为不饱和溶液,但是溶质质量不变,所以溶质质量分数不变变,选项B错误;
C、随加水量的增多,HA的pH变化大,说明HA的酸性强于HB,据越弱越水解的原则,NaB水解程度大,故NaA溶液的碱性弱于NaB溶液,pH小,选项C正确;
D、0.1000molL-1NaOH溶液滴定20.00mL 0.1000molL-1CH3COOH溶液,消氢氧化钠溶液体积为0时,醋酸为弱电解质,醋酸溶液的pH大于1,图象中醋酸的pH=1与实际不符,选项D错误;
答案选C。

练习册系列答案
相关题目
【题目】某同学用食用油进行实验,以下是实验操作和现象:
实验操作 | 将食用油滴入水中 | 向食用油中滴加溴水 | 将少量食用油与纯碱(主要成分是 |
实验现象 | 食用油浮在水面上 | 溴水褪色 | 分层现象消失 |
下列关于食用油的实验结论不正确的是( )
A.食用油的密度比水小
B.食用油中含碳碳不饱和键
C.食用油在碱性条件下会水解生成可溶于水的物质
D.食用油是一种有机酸