题目内容
下列措施对增大反应速率明显有效的是( )
| A.Na与无水乙醇反应时增大无水乙醇的用量 |
| B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,增大压强 |
| D.将炭块磨成炭粉用于燃烧 |
D
解析试题分析:A、增大无水乙醇的用量,反应物的浓度不变,反应速率不变,错误;B、浓硫酸和锌反应生成二氧化硫气体,错误;C、K2SO4与BaCl2两溶液反应的反应没有气体参加,而压强只改变有气体参加反应的化学反应速率,增大该反应的压强,反应速率不变,错误;D、固体的表面积越大,反应速率越大,将炭块磨成炭粉用于燃烧,反应速率增大,正确。
考点:本题考查反应速率的影响因素。

练习册系列答案
相关题目
决定化学反应速率的主要因素是
| A.催化剂 | B.参加反应的物质本身的性质 |
| C.反应物的浓度 | D.温度、压强以及反应物的接触面 |
已知X(g)+3Y(g)═ 2Z(g)△H>0,下列对该反应的说法中正确的是
| A.△S>0 |
| B.逆向能自发进行,且反应速率和平衡常数均较大 |
| C.反应物总能量大于生成物总能量 |
| D.在任何温度下都不能自发进行 |
下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)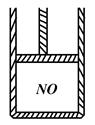
| A.等于1.369 g·L-1 |
| B.等于2.054 g·L-1 |
| C.在1.369g·L-1和2.054g·L-1之间 |
| D.在2.054g·L-1和4.108g·L-1之间 |
用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( )
| A.18O只存在于乙酸乙酯中 | B.18O存在于水、乙酸、乙醇以及乙酸乙酯中 |
| C.18O存在于乙酸乙酯、乙醇中 | D.若与丙酸反应生成酯的相对分子质量为102 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示: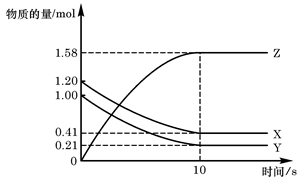
下列描述正确的是
| A.反应开始到10s,用Z表示的反应速率为0.158 mol·L-1·s-1 |
| B.反应开始到10s,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10s,Y的转化率为79.0% |
D.反应的化学方程式为:X(g) + Y(g) Z(g) Z(g) |
工业制硫酸中的一步重要反应是SO2(在400-500 C下的催化氧化:2SO2+O2
C下的催化氧化:2SO2+O2 2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法错误的是
2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法错误的是
| A.在上述条件下,SO2可能100%的转化为SO3 |
| B.使用催化剂是为了加快反应速率,提高生产效率 |
| C.达到平衡时,SO2与SO3的浓度保持不变 |
| D.为了提高SO2的转化率,可以适当提高O2的浓度 |
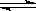 2Q(g)
2Q(g)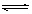 2C(g)(正反应吸热),下列图象中正确的是
2C(g)(正反应吸热),下列图象中正确的是