题目内容
13.将KClO3、I2各0.02mol加入12 克36.5%的盐酸中,I2恰好完全溶解,没有气体产生(不考虑盐酸的挥发).将反应后的溶液用冰水冷却,析出橙红色晶体A(A在常温下就有升华现象),过滤,将滤液蒸干,收集到KCl固体、8.7g液态水和极少量的A蒸气.则A的化学式可能是( )| A. | I2Cl6 | B. | ICl5 | C. | HClO | D. | KIO3 |
分析 橙红色晶体A在常温下就有升华现象,是共价化合物,不含钾元素,根据K元素守恒,可知最终收集的KCl为0.02mol,根据质量守恒计算A的质量,再根据Cl原子守恒、I原子守恒确定A中n(Cl)、n(I),进而确定是否含有O元素,结合原子物质的量之比确定化学式.
解答 解:橙红色晶体A在常温下就有升华现象,是共价化合物,不含钾元素,根据K元素守恒,可知最终收集的KCl为0.02mol,
根据质量守恒,可知A的质量=12g+0.02mol×122.5g/mol+0.02mol×254g/mol-8.7g-0.02mol×74.5g/mol=9.34g
根据Cl原子守恒,可知A中n(Cl)=0.02mol+$\frac{12g×36.5%}{36.5}$-0.02=0.12mol,
根据I原子守恒确定A中n(I)=0.04mol,故m(Cl)+m(I)=0.12mol×35.5g/mol+0.04mol×127g/mol=9.34g,
故A不含O元素,只由Cl、I两种元素组成,且n(I):n(Cl)=0.04mol:0.12mol=1:3,
则选项中只有A符合,
故选A.
点评 本题考查方程式的有关计算,题目难度中等,关键是利用守恒思想进行解答,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
1.向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正确的是( )
| A. | 钠熔化成小球 | |
| B. | 钠块沉在乙醇液面的下面 | |
| C. | 钠块在乙醇的液面上游动 | |
| D. | 钠块表面有气泡放出,有轻微爆炸产生 |
8.“钾泻盐”的化学式为MgSO4•KCl•xH2O,是一种制取钾肥的重要原料,它溶于水得到KCl与MgSO4的混合溶液.某化学活动小组设计了如下实验方案:以下说法不正确的是( )


| A. | 该方案能够计算出“钾泻盐”中KCl的质量分数 | |
| B. | 足量Ba(NO3)2溶液是为了与MgSO4充分反应 | |
| C. | “钾泻盐”化学式中x=3 | |
| D. | 上述实验数据的测定利用学校实验室里的托盘天平即可完成 |
18.侯氏制碱法制取纯碱的生产流程如图1所示:

某小组同学在实验室模拟该流程制纯碱,设计如下:
可供选择的试剂有:6mol•L-1盐酸、6mol•L-1硫酸、浓氨水、生石灰、石灰石、氯化铵、蒸馏水和冰.(夹持仪器略)
请回答:
(1)A装置中所装试剂是6mol/L 盐酸和石灰石,B装置的作用是除去CO2中的HCl.
(2)用相关化学用语说明D装置制取气体的原理氧化钙与水反应放热,使NH3•H2O分解产生NH3溶液中c(OH-)增大,使
NH3+H2O?NH3•H2O?NH4++OH-平衡逆向移动,利于NH3的逸出,CaO与水结合平衡逆向移动.
(3)检验D装置中产生的气体的方法从C中取出D装置导管,将湿润的红色石蕊试纸放于导管口处,若变蓝,则产生的气体为NH3.
(4)根据下表中四种物质的溶解度,回答:
①侯氏制碱是在30℃左右进行生产的,那么沉淀池中在3030℃C时析出的物质X是NaHCO3,分离方法过滤.C装置中反应的化学方程式是NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
②依据上表和工业流程图1,为了从C装置中分离后的溶液中得到更多的副产品NH4Cl,可采取的措施是a、c.
a.加NH3和NaCl b.通入CO2 c.降低温度
(5)C装置中产品X经煅烧得到纯碱,其中常含有少量的NaCl,为测定其纯度,某实验小组设计的以下方案正确的是②、③.
①取纯碱样品ag于试管中,溶解后,加入过量盐酸,用碱石灰吸收产生的气体,碱石灰增重bg.
②取纯碱样品ag于试管中,溶解后,先加入过量硝酸酸化,再滴加过量的AgNO3溶液,产生的沉淀经过滤、洗涤、干燥,称其质量为bg.
③取纯碱样品ag于试管中,溶解后,滴加过量的CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为bg.

某小组同学在实验室模拟该流程制纯碱,设计如下:
可供选择的试剂有:6mol•L-1盐酸、6mol•L-1硫酸、浓氨水、生石灰、石灰石、氯化铵、蒸馏水和冰.(夹持仪器略)
请回答:
(1)A装置中所装试剂是6mol/L 盐酸和石灰石,B装置的作用是除去CO2中的HCl.
(2)用相关化学用语说明D装置制取气体的原理氧化钙与水反应放热,使NH3•H2O分解产生NH3溶液中c(OH-)增大,使
NH3+H2O?NH3•H2O?NH4++OH-平衡逆向移动,利于NH3的逸出,CaO与水结合平衡逆向移动.
(3)检验D装置中产生的气体的方法从C中取出D装置导管,将湿润的红色石蕊试纸放于导管口处,若变蓝,则产生的气体为NH3.
(4)根据下表中四种物质的溶解度,回答:
 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 |
②依据上表和工业流程图1,为了从C装置中分离后的溶液中得到更多的副产品NH4Cl,可采取的措施是a、c.
a.加NH3和NaCl b.通入CO2 c.降低温度
(5)C装置中产品X经煅烧得到纯碱,其中常含有少量的NaCl,为测定其纯度,某实验小组设计的以下方案正确的是②、③.
①取纯碱样品ag于试管中,溶解后,加入过量盐酸,用碱石灰吸收产生的气体,碱石灰增重bg.
②取纯碱样品ag于试管中,溶解后,先加入过量硝酸酸化,再滴加过量的AgNO3溶液,产生的沉淀经过滤、洗涤、干燥,称其质量为bg.
③取纯碱样品ag于试管中,溶解后,滴加过量的CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为bg.
2.某化学反应:A(g)?B(g)+C(g),在温度为3 00K时,向2.0L恒容密闭容器中充入1.0mol A,反应过程中测得的B物质的物质的量随时间的变化关系如图,下列说法不正确的是( )


| A. | 0~50秒,A物质化学反应速率v(A)=0.0016mo 1•L-1•S-1 | |
| B. | 250s时该反应达到化学平衡状态 | |
| C. | 若改加入2.0mol A,A的平衡转化率大于20% | |
| D. | 300K时,该反应的平衡常数为0.025 mol•L-1 |
17.下列关于同系物的说法中,错误的是( )
| A. | 同系物具有相同的最简式 | |
| B. | 同系物之间相对分子质量相差14或14的整数倍 | |
| C. | 同系物符合同一通式 | |
| D. | 同系物的化学性质基本相似,物理性质随碳原子数的增加呈规律性变化 |
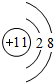 ,C的原子结构示意图是
,C的原子结构示意图是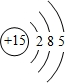 .
. 硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.