题目内容
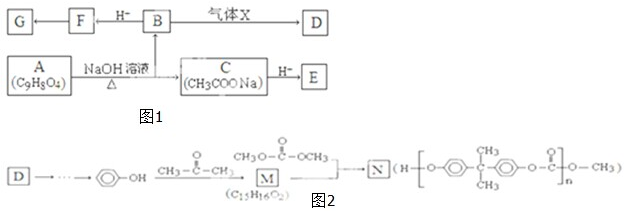
钛被称为21世纪金属,是研制卫星、火箭、宇宙飞船及深海潜艇的重要材料.研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置模拟获得金属钙(需定期更换石墨棒),并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )
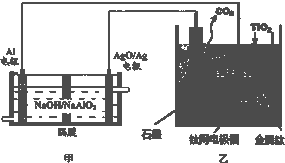

| A、甲装置工作过程中OH-向AgO/Ag极移动;乙装置工作过程中O2-向阴极移动 | ||
| B、乙装置阳极的电极反应式为C+2O2--4e-═CO2↑ | ||
C、若电解金属钛效率为η,则获取1mol Ti时消耗Al的物质的量
| ||
| D、在制备金属钛前后,整套装置中CaO的总量减少 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据图知,甲为原电池,Al为负极,被氧化,AgO/Ag极为正极,发生还原反应,乙为电解装置,阳极上电极反应式为C+2O2--4e-═CO2↑,阴极上电极反应式为:2Ca2++4e-═2Ca,钙还原二氧化钛反应方程式为:2Ca+TiO2=Ti+2CaO,以此解答该题.
解答:
解:A.甲装置工作过程中OH-向负极移动,即向Al极移动,乙装置工作过程中O2-向阳极移动,故A错误;
B.C为阳极,被氧化,阳极上电极反应式为C+2O2--4e-═CO2↑,故B正确;
C.若电解金属钛效率为η,获取1mol Ti需要电子的物质的量为
mol,消耗Al的物质的量
mol,故C错误;
D.阴极上电极反应式为:2Ca2++4e-═2Ca,钙还原二氧化钛反应方程式为:2Ca+TiO2=Ti+2CaO,在制备金属钛前后,整套装置中CaO的总量不变,故D错误.
故选B.
B.C为阳极,被氧化,阳极上电极反应式为C+2O2--4e-═CO2↑,故B正确;
C.若电解金属钛效率为η,获取1mol Ti需要电子的物质的量为
| 4 |
| η |
| 4 |
| 3η |
D.阴极上电极反应式为:2Ca2++4e-═2Ca,钙还原二氧化钛反应方程式为:2Ca+TiO2=Ti+2CaO,在制备金属钛前后,整套装置中CaO的总量不变,故D错误.
故选B.
点评:本题综合考查电解池和原电池知识,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握电极方程式的书写,为解答该类题目的关键,难度中等.

练习册系列答案
相关题目
绿色化学对于化学反应提出了“原子经济性”的要求.理想的原子经济性反应是原料中的原子全部转化为产物,不产生副产品,实现零排放.下列几种生产乙苯的方法中,原子经济性最好的是( )
A、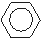 +C2H5Cl→ +C2H5Cl→ +HCl +HCl |
B、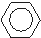 +C2H5OH→ +C2H5OH→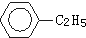 +H2O +H2O |
C、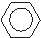 +CH2═CH2→ +CH2═CH2→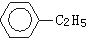 |
D、 +CH3CH3→ +CH3CH3→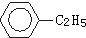 +HCl +HCl |
已知H2(g)+Br2(g)→2HBr(g)+72kJ.1mol Br2(g)液化放出的能量为30kJ,其它相关数据如下表:
则上述表格中的a值为( )
| H2(g) | Br2(l) | HBr(g) | |
| 1mol 分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、404 | B、344 |
| C、260 | D、200 |
下列说法正确的是( )
| A、常温下,等物质的量浓度的三种溶液①(NH4)2CO3②NH4Cl③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
| B、等物质的量浓度的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| C、常温下,在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、S2-、AlO2-、SO32-等离子不可能大量共存 |
| D、一定温度下,将盐酸滴加入醋酸钠溶液中至呈中性.此时溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
某物质灼烧时焰色反应为黄色,下列判断正确的是( )
| A、该物质一定是钠的化合物 |
| B、该物质一定含钠元素 |
| C、该物质一定是金属钠 |
| D、以上说法都不对 |
下列化学(或离子)方程式中,不正确的是( )
A、为减少煤燃烧产生SO2,用CaCO3脱硫:2CaCO3+O2+2SO2
| ||||
| B、碳酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-═NH3?H2O | ||||
| C、从酸化的海带灰浸出液中提取碘:2I-+2H++H2O2═I2+2H2O | ||||
D、将Na2CO3加热至熔融不能选用石英坩埚:SiO2+Na2CO3
|
如图是某盐酸试剂标签部分内容,据此判断( )


| A、该盐酸与钠可存放在同一药品橱柜中 |
| B、该盐酸含HCl质量为600g |
| C、配制100mL 0.2mol/L盐酸需用到玻璃仪器为量简、烧杯、玻璃棒 |
| D、该盐酸的物质的量浓度为12.0mol/L |