题目内容
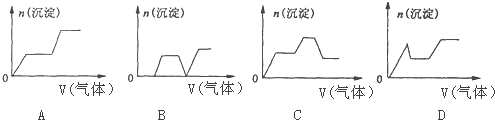
12. 向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成Al (OH)3沉淀的量随ALCL3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成Al (OH)3沉淀的量随ALCL3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液中:Na+、Fe3+、SO4-、HCO3- | |
| B. | b点对应的溶液中:Na+、S2-、SO42-、Cl- | |
| C. | c点对应的溶液中:Ag+、Ca2+、NO3-、F- | |
| D. | d点对应的溶液中:K+、NH4+、CO32-、I- |
分析 A.a点溶液显碱性,NaOH过量,铁离子与碳酸氢根离子发生双水解反应,且二者能够与氢氧根离子反应;
B.b点恰好生成偏铝酸钠,四种离子之间不反应,都不与偏铝酸钠反应;
C.c点偏铝酸钠与氯化铝恰好完全反应生成氢氧化铝和氯化钠,银离子与氯离子反应生成氯化银沉淀;
D.d点为氯化铝溶液,碳酸根离子与铝离子发生双水解反应.
解答 解:A.a点溶液显碱性,NaOH过量,则不可能存在Fe3+、HCO3-,不能共存,故A错误;
B.b点恰好生成偏铝酸钠,溶液显碱性,该组离子之间不反应,能大量共存,故B正确;
C.c点偏铝酸钠与氯化铝恰好完全反应生成氢氧化铝,还生成氯化钠,则不可能存在Ag+,不能共存,故C错误;
D.d点为氯化铝溶液,Al3+、CO32-相互促进水解生成沉淀和气体,则不能共存,故D错误;
故选B.
点评 本题考查离子共存的判断,题目难度中等,明确图象中各点对应的反应及溶液的成分、离子之间的反应是解答的关键,注意选项A中的相互促进水解反应.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
3.下列化学用语使用正确的是( )
| A. | 乙烯的球棍模型为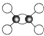 | |
| B. | H2O2的电子式为 | |
| C. | 甲烷的结构式为CH4 | |
| D. | 乙酸乙酯的结构简式为CH3COOCH3CH2 |
20.a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种.已知:
①a、c皆能与稀硫酸反应放出气体;
②b与d的硝酸盐反应,置换出单质d;
③c与强碱反应放出气体;
④c、e在冷浓硫酸中发生钝化.由此可判断a、b、c、d、e依次为( )
①a、c皆能与稀硫酸反应放出气体;
②b与d的硝酸盐反应,置换出单质d;
③c与强碱反应放出气体;
④c、e在冷浓硫酸中发生钝化.由此可判断a、b、c、d、e依次为( )
| A. | Fe Cu Al Ag Mg | B. | Al Cu Mg Ag Fe | ||
| C. | Mg Cu Al Ag Fe | D. | Mg Ag Al Cu Fe |
7.下列说法中,正确的是( )
| A. | 原子最外层电子数为2的元素一定是金属元素 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性都依次增强 | |
| C. | 金属氧化物就是碱性氧化物 | |
| D. | 化合物XY3中,X可能呈-3价,Y可能呈+1价 |
4.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )


| A. | 该硫酸的物质的量浓度为9.2 mol•L-1 | |
| B. | 1 mol 铁加入到足量的该硫酸中,可产生2 g H2 | |
| C. | 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol•L-1 | |
| D. | 配制200 mL 4.6 mol•L-1的硫酸溶液需取该硫酸50 mL |
1.某澄清溶液中只含有以下可能存在的若干种离子:Na+、Fe3+、Fe2+、SO42-、Cl-、Ba2+、I-.现取部
分溶液依次进行如下实验:①通入一定量氯气后,加入CCl4振荡,静置后CCl4层呈紫红色,用分液漏斗
分液;②向分液后的水溶液中加入足量硝酸酸化的硝酸钡溶液,产生白色沉淀;③过滤后将滤液分为两份,
向一份中加入硝酸酸化的硝酸银溶液,产生大量沉淀,向另一份中加入少量KSCN溶液,溶液立即变为红
色.根据上述实验,以下推测正确的是( )
分溶液依次进行如下实验:①通入一定量氯气后,加入CCl4振荡,静置后CCl4层呈紫红色,用分液漏斗
分液;②向分液后的水溶液中加入足量硝酸酸化的硝酸钡溶液,产生白色沉淀;③过滤后将滤液分为两份,
向一份中加入硝酸酸化的硝酸银溶液,产生大量沉淀,向另一份中加入少量KSCN溶液,溶液立即变为红
色.根据上述实验,以下推测正确的是( )
| A. | 原溶液一定显中性 | |
| B. | 原溶液中肯定不存在的离子有Fe2+、Ba2+ | |
| C. | 无法确定原溶液中是否存在Cl-、Na+、SO42- | |
| D. | 原溶液中肯定存在的离子有Fe2+、SO42-、I- |
2.有两种气态不饱和烃的混合物共20mL,完全燃烧可生成H2O蒸气72mL和CO276mL(气体体积均在同温同压下测定),则这两种烃的分子式为( )
| A. | C2H4、C4H8 | B. | C2H2、C3H8 | C. | C3H4、C4H8 | D. | C3H4、C3H8 |