题目内容
20.下列电离方程式错误的是( )| A. | Al2(SO4)3=2Al3++3SO42- | B. | Na2CO3=Na++CO32- | ||
| C. | Ba(OH)2=Ba2++2 OH- | D. | NaHSO4=Na++H++SO42- |
分析 弱电解质在水溶液里部分电离写“?”,强电解质在水溶液里完全电离“=”,电解质在水溶液里电离生成阴阳离子,多元弱酸分步电离,多元弱碱电离写一步电离方程式,据此分析解答.
解答 解:A、硫酸铝是强电解质,能完全电离,电离方程式为:Al2(SO4)3=2Al3++3SO42-,故A不选;
B、碳酸钠是强电解质,能完全电离,电离方程式为:Na2CO3=2Na++CO32-,故B选;
C、氢氧化钡是强电解质,能完全电离,电离方程式为:Ba(OH)2=Ba2++2OH-,故C不选;
D、硫酸氢钠在水溶液中完全电离,电离方程式为:NaHSO4=Na++H++SO42-,故D不选.
故选B.
点评 本题主要考查电离方程式书写,掌握正确书写电离方程式的方法,并能正确判断电离方程式的正误是解答关键,注意多元弱酸分步电离,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
10.孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物.某工厂以孔雀石为主要原料制备CuSO4•5H2O及纳米材料G,主要步骤如下:
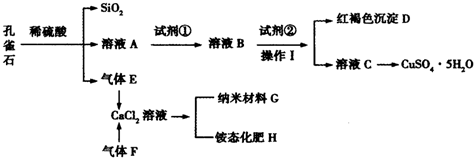
已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+沉淀完全.Fe3+、Fe2+、Cu2+开始沉淀及完全沉淀的pH分别如下:
请回答下列问题:
(1)孔雀石主要成分Cu2(OH)2CO3与稀硫酸反应的化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑.
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+.要检验其中的Fe2+应选择下列试剂中的a(填序号).
a.KMnO4 b.NaOH C.H2O2 d.KSCN
(3)试剂①是一种氧化剂,加入该氧化剂的作用是将溶液中的Fe2+氧化为Fe3+(以便在Cu(OH)2沉淀之前,通过调节溶液pH使Fe(OH)3沉淀完全);
(4)向溶液B中加入试剂②的化学式为CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3.
(5)气体E和气体F应该先通入CaCl2溶液中的是NH3(填化学式).写出制备G和H的化学反应方程式2NH3+CO2+CaCl2+H2O═CaCO3↓+2NH4Cl.
(6)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-还原为Mn2+,则该反应的离子方程式为MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.取A溶液20.00mL,用去0.0240mol/L KMnO4溶液16.00mL时,恰好达到滴定终点,则A溶液中Fe2+浓度为0.0960mol/L.

已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+沉淀完全.Fe3+、Fe2+、Cu2+开始沉淀及完全沉淀的pH分别如下:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
(1)孔雀石主要成分Cu2(OH)2CO3与稀硫酸反应的化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑.
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+.要检验其中的Fe2+应选择下列试剂中的a(填序号).
a.KMnO4 b.NaOH C.H2O2 d.KSCN
(3)试剂①是一种氧化剂,加入该氧化剂的作用是将溶液中的Fe2+氧化为Fe3+(以便在Cu(OH)2沉淀之前,通过调节溶液pH使Fe(OH)3沉淀完全);
(4)向溶液B中加入试剂②的化学式为CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3.
(5)气体E和气体F应该先通入CaCl2溶液中的是NH3(填化学式).写出制备G和H的化学反应方程式2NH3+CO2+CaCl2+H2O═CaCO3↓+2NH4Cl.
(6)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-还原为Mn2+,则该反应的离子方程式为MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.取A溶液20.00mL,用去0.0240mol/L KMnO4溶液16.00mL时,恰好达到滴定终点,则A溶液中Fe2+浓度为0.0960mol/L.
11.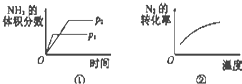 对于可逆反应N2(g)+3H2(g)?2NH3(g)该反应是放热反应,下列各项对示意图的解释与图象相符的是( )
对于可逆反应N2(g)+3H2(g)?2NH3(g)该反应是放热反应,下列各项对示意图的解释与图象相符的是( )
 对于可逆反应N2(g)+3H2(g)?2NH3(g)该反应是放热反应,下列各项对示意图的解释与图象相符的是( )
对于可逆反应N2(g)+3H2(g)?2NH3(g)该反应是放热反应,下列各项对示意图的解释与图象相符的是( )| A. | ②温度对反应的影响 | B. | ④催化剂对反应的影响 | ||
| C. | ①压强对反应的影响(p2>p1) | D. | ③平衡体系增加N2对反应的影响 |
15.某二价金属A与稀硝酸反应时,A与硝酸所消耗的物质的量比为2﹕5,则硝酸被还原的产物可能是( )
| A. | NO | B. | NO2 | C. | N2O3 | D. | NH4NO3 |
5.下列措施不能达到节能减排目的是( )
| A. | 利用太阳能制氢燃料 | B. | 多乘坐公交车少开私家车 | ||
| C. | 利用燃烧煤发电 | D. | 用节能灯代替白炽灯 |
12.下列解释物质用途或现象的反应方程式不准确的是( )
| A. | 硫酸型酸雨的形成会涉及反应:2H2SO3+O2$\frac{\underline{\;催化剂\;}}{\;}$2H2SO4 | |
| B. | 氯化铝溶液中加入过量的氨水 Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| D. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H2O |