题目内容
10.孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物.某工厂以孔雀石为主要原料制备CuSO4•5H2O及纳米材料G,主要步骤如下: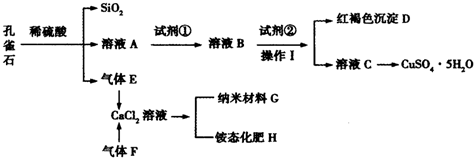
已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+沉淀完全.Fe3+、Fe2+、Cu2+开始沉淀及完全沉淀的pH分别如下:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
(1)孔雀石主要成分Cu2(OH)2CO3与稀硫酸反应的化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑.
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+.要检验其中的Fe2+应选择下列试剂中的a(填序号).
a.KMnO4 b.NaOH C.H2O2 d.KSCN
(3)试剂①是一种氧化剂,加入该氧化剂的作用是将溶液中的Fe2+氧化为Fe3+(以便在Cu(OH)2沉淀之前,通过调节溶液pH使Fe(OH)3沉淀完全);
(4)向溶液B中加入试剂②的化学式为CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3.
(5)气体E和气体F应该先通入CaCl2溶液中的是NH3(填化学式).写出制备G和H的化学反应方程式2NH3+CO2+CaCl2+H2O═CaCO3↓+2NH4Cl.
(6)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-还原为Mn2+,则该反应的离子方程式为MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.取A溶液20.00mL,用去0.0240mol/L KMnO4溶液16.00mL时,恰好达到滴定终点,则A溶液中Fe2+浓度为0.0960mol/L.
分析 孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,向孔雀石中加入足量稀硫酸,发生的反应有Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,Fe+H2SO4=FeSO4+H2↑,硅和稀硫酸不反应,溶液A只含Cu2+、Fe2+两种金属离子,然后过滤得到的滤渣中含有Si的氧化物,溶液A中含有含有铁盐和亚铁盐及硫酸铜,气体E为CO2、H2,通入氨气,2NH3+CO2+CaCl2+H2O═CaCO3↓+2NH4Cl,制备氯化铵,向溶液A中加入试剂①得到溶液B,试剂①是一种氧化剂,将Fe2+转化为Fe3+且不能引进杂质,可选取双氧水,向溶液B中加入试剂②经过操作Ⅰ得到溶液C和红褐色沉淀D,则操作Ⅰ为过滤,D为Fe(OH)3,以及过量的试剂,溶液C为硫酸铜溶液,所以为试剂②为CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3,据此答题.
(1)碱式碳酸铜能与稀硫酸反应生成硫酸铜、水和二氧化碳;
(2)Fe2+具有还原性,可使高锰酸钾溶液褪色,高锰酸钾溶液与Cu2+、Fe3+不反应,NaOH 与Cu2+、Fe2+、Fe3+都反应,无法鉴别,H2O2 与Fe2+反应无明显现象,Fe2+与KSCN不反应;
(3)试剂①是一种氧化剂,将Fe2+转化为Fe3+且不能引进杂质,以便在Cu(OH)2沉淀之前,通过调节溶液pH使Fe(OH)3沉淀完全;
(4)溶液B加入CuO调节溶液pH值,使Fe3+的水解生成氢氧化铁沉淀而除去,调节溶液的PH,除去铁离子杂质;
(5)根据流程图知,生成的气体E为二氧化碳、氢气,制取铵盐需通氨气,根据侯氏制碱法原理分析;
(6)氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目,Fe2+溶液与KMnO4溶液发生氧化还原反应,反应中MnO4-被还原为Mn2+,结合原子守恒和电荷守恒配平书写;根据MnO4-~5Fe2+,计算A溶液中Fe2+浓度.
解答 解:(1)碱式碳酸铜为碱式盐能与稀硫酸反应:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,生成硫酸铜、水和二氧化碳,
故答案为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(2)Fe2+具有还原性,可被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,与KSCN不反应,加入氢氧化钠溶液可生成氢氧化铁、氢氧化铜沉淀而不能检验Fe2+,双氧水,双氧水是一种绿色试剂,将Fe2+氧化为Fe3+,但无明显现象,只有a正确,
故答案为:a;
(3)试剂①是一种氧化剂,将Fe2+转化为Fe3+且不能引进杂质,可选取双氧水,以便在Cu(OH)2沉淀之前,通过调节溶液pH使Fe(OH)3沉淀完全,
故答案为:将溶液中的Fe2+氧化为Fe3+(以便在Cu(OH)2沉淀之前,通过调节溶液pH使Fe(OH)3沉淀完全)
(4)在溶液B中加CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等调节溶液的pH使Fe3+完全沉淀,且不引入新的杂质,根据表中数据,Fe3+完全沉淀时PH的范围是2.2~3.2,
故答案为:CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3;
(5)根据流程图知,生成的气体E为二氧化碳、氢气,在氯化钙溶液中通入气体F为氨气制备碳酸钙纳米材料,因为二氧化碳不与氯化钙溶液反应,同时二氧化碳在水中的溶解度很小,因此,要先向氯化钙溶液中加入氨水或通入氨气,在碱性溶液中通入二氧化碳,增加二氧化碳的溶解度,从而生成碳酸钙,反应方程式为:2NH3+CO2+CaCl2+H2O=CaCO3↓+2NH4Cl,
故答案为:NH3;2NH3+CO2+H2O+CaCl2→CaCO3↓+2NH4Cl;
(6)Fe2+溶液与KMnO4溶液发生氧化还原反应,反应中MnO4-被还原为Mn2+,最小公倍数为5,所以KMnO4前系数为1,Fe2+前系数为5,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,根据离子方程可知MnO4-~5Fe2+,用去 KMnO4的物质的量为16.00mL×0.0240mol/L=3.84×10-4mol,所以A溶液中Fe2+浓度为$\frac{3.84×1{0}^{-4}mol×5}{0.02L}$=0.096mol/L,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;0.096mol/L.
点评 本题考查以孔雀石为主要原料制备CuSO4•5H2O及纳米材料,为高频考点和常见题型,侧重于学生的分析、实验和计算能力得到考查,注意把握实验的原理以及物质的性质,为解答该类题目的关键,注意掌握实验基本操作和流程分析,题目难度中等.

| A. | 配制1L该溶液,可将0.1mol CaCl2溶于1L水中 | |
| B. | Ca2+和Cl-的物质的量浓度都是0.1mol•L-1 | |
| C. | 从试剂瓶中取该溶液的一半,则所取溶液的物质的量浓度为0.05mol•L-1 | |
| D. | 将该瓶溶液稀释一倍,则所得溶液的c(Cl-)为0.1mol•L-1 |
| A. | 13.2mol•L-1 | B. | 5.85mol•L-1 | C. | 23.4mol•L-1 | D. | 11.7mol•L-1 |
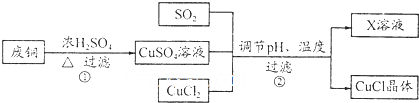
(l)写出过程①的主要化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)分析下表,析出CuCl晶体时的最佳pH为2;当pH较大时,CuCI晶体产率较低,其原因是pH增大,Cu2+水解损失增加.
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率(%) | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
(4)为了更好体现绿色化学思想,有人提出如下方案:方案一:可将上述X稀溶液用于废铜的处理(如图所示),则Y可以为O2(填化学式).
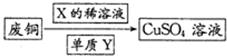
方案二:①中Cu与浓H2SO4反应所得SO2和CuSO4用于②中CuCl的制备,理论上不需要(“需要”或“不需要”)另外补充SO2,原因是反应①Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O中生成的CuSO4和SO2的物质的量之比为1:1,而反应②CuSO4+CuCl2+SO2+2H2O═2Cucl↓+2H2SO4需要的CuSO4和SO2的物质的量之比也恰好为1:1,所以理论上不需要补充SO2(结合化学方程式回答).
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p1 原子半径④>①>③>② | |
| B. | 具有下列价电子排布式的原子中,①1s22s22p63s2;②1s22s22p63s23p1;③1s22s2 2p3;④1s22s22p4.第一电离能:③>④>①>② | |
| C. | ①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ | |
| D. | 某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17 995、21703,当它与氯气反应时可能生成的阳离子是X3+ |
| A. | Al2(SO4)3=2Al3++3SO42- | B. | Na2CO3=Na++CO32- | ||
| C. | Ba(OH)2=Ba2++2 OH- | D. | NaHSO4=Na++H++SO42- |