题目内容
9.在下列物质中:①碘②烧碱③NaCl④干冰⑤氯化氢⑥Na2O2.用序号填写下列空白:(1)既含有离子键又含有非极性键的化合物是⑥;
(2)仅含有离子键的化合物是③;
(3)仅含有共价键的单质是①④⑤.
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,据此分析解答.
解答 解:①碘单质中只含共价键;
②烧碱中钠离子和氢氧根离子间存在离子键,氧原子和氢原子之间存在极性共价键;
③NaCl中钠离子和氯离子之间存在离子键;
④干冰分子中氧原子和碳原子之间存在共价键;
⑤氯化氢中氯原子和氢原子之间存在共价键;
⑥Na2O2中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在非极性共价键;
故答案为:(1)⑥(2)③(3)①④⑤.
点评 本题考查了化学键的判断,注意离子键和共价键的区别,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.以下有关元素性质的说法不正确的是( )
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p1 原子半径④>①>③>② | |
| B. | 具有下列价电子排布式的原子中,①1s22s22p63s2;②1s22s22p63s23p1;③1s22s2 2p3;④1s22s22p4.第一电离能:③>④>①>② | |
| C. | ①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ | |
| D. | 某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17 995、21703,当它与氯气反应时可能生成的阳离子是X3+ |
20.下列电离方程式错误的是( )
| A. | Al2(SO4)3=2Al3++3SO42- | B. | Na2CO3=Na++CO32- | ||
| C. | Ba(OH)2=Ba2++2 OH- | D. | NaHSO4=Na++H++SO42- |
17.下列实验装置图所示的实验操作,正确的是( )
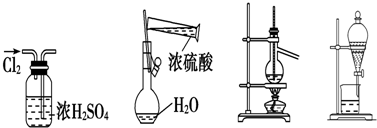

| A. | 干燥Cl2 | B. | 配制硫酸溶液 | C. | 蒸馏 | D. | 分液 |
4.下列各组离子在溶液中可大量共存的是( )
| A. | K+,Cl-,CO32-,Na+ | B. | H+,Ba2+,Fe3+,S2- | ||
| C. | NH4+,SO42-,K+,OH- | D. | H+,NO3-,Na+,SiO32- |
14.下列反应的离子方程式表示正确的是( )
| A. | 将过量的铁丝投入稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | 硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| C. | NH4HCO3溶液与过量的NaOH溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 小苏打溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32 |
1.下列物质属于糖类且属于高分子化合物的是( )
| A. | 葡萄糖 | B. | 花生油 | C. | 蛋白质 | D. | 淀粉 |
18.对于可逆反应2SO2 (g)+O2(g)?2SO3(g)△H<0在一定温度下其平衡数为K,下列说法正确的是( )
| A. | 增大SO2的转化率K值一定增大 | B. | 减小压强K值减小 | ||
| C. | 升高温度K值增大 | D. | K值越大SO2转化率越大 |
19.下列反应中二氧化硫被氧化的是( )
| A. | SO2+2H2S═3S+2H2O | B. | SO2+2NaOH═Na2SO3+H2O | ||
| C. | SO2+H2O═H2SO3 | D. | SO2+Cl2+2H2O═4H++2Cl-+SO42- |