题目内容
17.下列变化过程中,克服了分子间作用力的是( )| A. | 食盐熔化 | B. | 氯化氢溶于水 | C. | 干冰气化 | D. | 金属钠熔化 |
分析 只有分子晶体存在分子间作用力,一般来说,当分子晶体聚集状态改变或溶于水时,且为非电解质时克服分子间作用力,以此解答该题.
解答 解:A.食盐是离子晶体,微粒间的作用力是离子键,故A错误;
B.氯化氢溶于水克服共价键,故B错误;
C.干冰为分子晶体,气化克服分子间作用力,故C正确;
D.钠为金属晶体,熔化克服金属键,故D错误.
故选C.
点评 本题考查了晶体类型和微粒之间的作用力,为高频考点,此类题的解题方法是:先判断晶体类型,再判断克服的作用力.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
7.实验室利用冰醋酸和正丁醇制备乙酸正丁酯,实验装置如图1所示,可能用到的有关数据如下表:
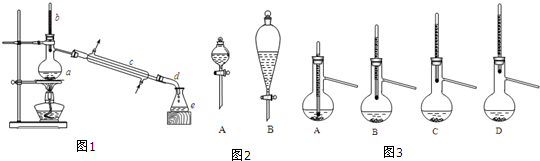
合成反应:在干燥的a中加入9.32g正丁醇、7.2mL 冰醋酸和3~4滴浓硫酸,摇匀后,加几粒沸石,c中通水,开始缓慢加热,控制馏出物的温度不超过130℃.
分离提纯:①将仪器a中反应后的混合液与仪器e中的馏出物合并,转入分液漏斗中;②依次用水、少量的10%碳酸钠溶液和水洗涤,分离后再加干燥剂M,静置一段时间后,弃去M;③将最终得到的反应粗产物转入洗净的仪器a中,加入几粒沸石,进行蒸馏,得到乙酸正丁酯7.31g.
请回答下列问题:
(1)仪器a的名称是蒸馏烧瓶.
(2)在分液时应选如图2装置中的B(填序号),使用该仪器前应先检漏.
(3)写出制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
(4)第一次水洗的目的是除去硫酸及部分乙酸.
(5)干燥剂M可以是B(填序号)
A.五氧化二磷 B.无水硫酸钠 C.碱石灰 D.氢氧化钠固体
(6)步骤③得到的粗产品蒸馏提纯时,图3所示装置中,温度计位置可能导致收集到的产品中混有高沸点杂质的装置为D(填序号)
(7)本实验所得到的乙酸正丁酯的产率是C(填序号)
A.30% B.40% C.50% D.55%

| 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 | |
| 密度/(g/cm3) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 118.0 | 118.1 | 126.1 | 142 |
分离提纯:①将仪器a中反应后的混合液与仪器e中的馏出物合并,转入分液漏斗中;②依次用水、少量的10%碳酸钠溶液和水洗涤,分离后再加干燥剂M,静置一段时间后,弃去M;③将最终得到的反应粗产物转入洗净的仪器a中,加入几粒沸石,进行蒸馏,得到乙酸正丁酯7.31g.
请回答下列问题:
(1)仪器a的名称是蒸馏烧瓶.
(2)在分液时应选如图2装置中的B(填序号),使用该仪器前应先检漏.
(3)写出制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
(4)第一次水洗的目的是除去硫酸及部分乙酸.
(5)干燥剂M可以是B(填序号)
A.五氧化二磷 B.无水硫酸钠 C.碱石灰 D.氢氧化钠固体
(6)步骤③得到的粗产品蒸馏提纯时,图3所示装置中,温度计位置可能导致收集到的产品中混有高沸点杂质的装置为D(填序号)
(7)本实验所得到的乙酸正丁酯的产率是C(填序号)
A.30% B.40% C.50% D.55%
8.下列递变情况中,正确的是( )
| A. | Na、Mg、Al原子最外层电子数依次减少 | |
| B. | C、N、O元素非金属性依次增强 | |
| C. | C、N、O元素最高正价依次增大 | |
| D. | Li、Na、K的金属性依次减弱 |
5.下列各组内的物质,属于同系物的是( )
| A. | 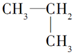 与 与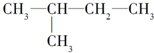 | B. | 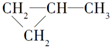 与 与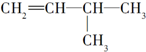 | ||
| C. | HO-CH2-CH2-OH与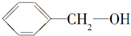 | D. | 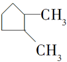 与 与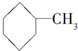 |
2.已知反应方程式:NH4NO3+Zn═ZnO+N2↑+2H2O,下列有关说法中正确的是( )
| A. | 该反应中NH4NO3只作氧化剂 | |
| B. | ZnO是还原产物 | |
| C. | 氧化产物只有N2 | |
| D. | 该反应每生成1mol N2转移5mol电子 |
9.氢气可以在氧气中燃烧.在该反应中:断裂1mol H-H键消耗的能量为Q1kJ,断裂1mol O=O键消耗的能量为Q2kJ,形成1mol H-O键释放的能量为Q3 kJ.下列关系式中,正确的是( )
| A. | 2Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
6.下列反应属于吸热反应的是( )
| A. | 金属镁与盐酸反应 | B. | 石灰石高温分解 | ||
| C. | 盐酸与氢氧化钠溶液反应 | D. | 二氧化硫和氧气生成三氧化硫 |
7.某学生为了探究锌与盐酸反应过程中的速率变化.在100mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如表:
(1)解释2min~3min反应速率最大的原因该反应是放热反应,2min~3min时溶液温度最高,反应速率最快;反应速率最小的时间段是4min~5min,原因为此时反应物的浓度最小,反应速率最慢.
(2)在4min~5min时间段内,用盐酸的浓度变化表示的反应速率为0.02mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A.Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是A、C、D.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50.0 | 120.0 | 232.0 | 290.0 | 312.4 |
(2)在4min~5min时间段内,用盐酸的浓度变化表示的反应速率为0.02mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A.Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是A、C、D.
 ;物质⑤的结构式O=C=O.
;物质⑤的结构式O=C=O.