题目内容
【题目】下列关于焓变![]() 的叙述或判断正确的是
的叙述或判断正确的是![]()
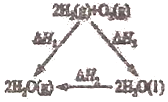
A.据如图可知:![]()
B.由![]() 可知,若将含1mol
可知,若将含1mol![]() 的稀溶液与含1molNaOH的稀溶液混合,放出的热量为
的稀溶液与含1molNaOH的稀溶液混合,放出的热量为![]()
C.![]() 、30MPa下,将
、30MPa下,将![]() 和
和![]() 置于密闭容器中充分反应,放出
置于密闭容器中充分反应,放出![]() 热量,则反应
热量,则反应![]() 的
的![]()
D.![]() 在常温下能自发进行,则该反应的
在常温下能自发进行,则该反应的![]()
【答案】D
【解析】
![]() 由盖斯定律可知,反应一步完成与分步完成的热效应相同,由图可知
由盖斯定律可知,反应一步完成与分步完成的热效应相同,由图可知![]() ,故A错误;
,故A错误;
B.醋酸电离吸热,则将含![]() 的稀溶液与含
的稀溶液与含![]() 的稀溶液混合,放出的热量小于
的稀溶液混合,放出的热量小于![]() ,故B错误;
,故B错误;
C.合成氨为放热反应,热化学方程式中为完全转化时的能量变化,将![]() 和
和![]() 置于密闭容器中充分反应,放出
置于密闭容器中充分反应,放出![]() 热量,1mol氮气完全反应放热大于
热量,1mol氮气完全反应放热大于![]() ,则反应
,则反应![]() 的
的![]() ,故C错误;
,故C错误;
D.![]() 的反应可自发进行,
的反应可自发进行,![]() ,在常温下能自发进行,则该反应的
,在常温下能自发进行,则该反应的![]() ,故D正确;
,故D正确;
故选D。

【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300 ℃以上完全分解 ②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
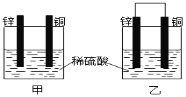
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。
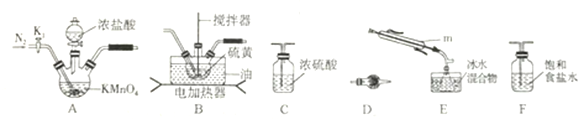
①仪器m 的名称为__________,装置F 中试剂的作用是_________。
②装置连接顺序: A![]() ______
______![]()
![]()
![]() E
E![]() D。
D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是_____________。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和____________。
(2)少量S2Cl2泄漏时应喷水雾减慢其挥发(或扩散),并产生酸性悬浊液,但不要对泄漏物或泄漏点直接喷水,其原因是______________。
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。
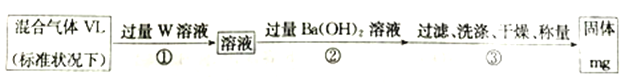
①W溶液可以是_____(填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为_________(用含V、m 的式子表示)。