题目内容
4.下表是元素周期表的一部分,元素Z为短周期元素,R的一种核素在考古时常用于鉴定一些文物的年代.下列叙述中正确的是( )| R | X | |||
| W | Y | Z |
| A. | W的氧化物属于酸性氧化物,与一切酸都不能发生反应 | |
| B. | Z的单质可用于杀灭田鼠 | |
| C. | Y、Z的最高价氧化物对应的水化物的酸性:Y>Z | |
| D. | X、Y的氢化物的沸点:Y>X |
分析 元素Z为短周期元素,可知各元素都处于短周期,R的一种核素在考古时常用于鉴定一些文物的年代,可推知R为C;由元素在周期表中的位置可知,W为Si、X为N、Y为P、Z为Cl元素,然后结合元素周期律与元素化合物性质解答.
解答 解:元素Z为短周期元素,可知元素都处于短周期,R的一种核素在考古时常用于鉴定一些文物的年代,可推知R为C;由元素在周期表中的位置可知,W为Si、X为N、Y为P、Z为Cl,
A.W的氧化物为二氧化硅,二氧化硅为酸性氧化物,但是二氧化硅能与氢氟酸反应,故A错误;
B.Z为Cl元素,氯气有毒,可用于灭鼠,故B正确;
C.同周期随原子序数增大非金属性减弱,故非金属性Z>Y,故最高价氧化物对应的水化物大小为:Z>Y,故C错误;
D.X、Y分别为N、P,用于氨气分子中存在氢键,则氨气的沸点较高,故D错误;
故选B.
点评 本题考查元素周期表与元素周期律的应用,题目难度中等,推断突破口为R的一种核素用于考古,注意掌握元素周期表的结构、元素周期律的内容.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
14.下列说法正确的是( )
| A. | 当今化学研究的方向是研究化学反应中原子的守恒关系 | |
| B. | 光导纤维由硅晶体制成,具有耐腐蚀、传输能力强等特点 | |
| C. | 煤在燃烧过程中要放出大量SO2,是引起光化学烟雾的“罪魁祸首” | |
| D. | 禽流感并不可怕,当加热到70℃以上或使用日常消毒剂都可使其病毒蛋白变性而致死 |
15.下列化学用语正确的是( )
| A. | 氯化钠的电子式: | |
| B. | 聚氯乙烯的结构简式: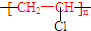 | |
| C. | 硫离子的结构示意图: | |
| D. | 碳酸氢铵的电离方程式:NH4HCO3=NH4++H++CO32ˉ |
12.已知25℃时,电离常数Ka(HF)=3.6×10-4mol•L-1,溶度积常数Ksp(CaF2)=1.46×10-10,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.O×10一16.下列说法正确的是( )
| A. | 25℃时,O.1 mol•L-1HF溶液pH=l,Ksp(CaF2)随温度和浓度的变化而变化 | |
| B. | 向1L0.2 mol•L-1HF溶液中加入1L O.2 mol•L-1CaCl2溶液,没有沉淀产生 | |
| C. | AgCl不溶于水,不能转化为AgI | |
| D. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于$\frac{1}{\sqrt{1.8}}$×10-11mol•L-1 |
9.向Ba(OH)2和NaOH混合溶液中缓缓通入CO2气体至过量,生成沉淀物质的量与通入CO2气体的体积V(标准状况)的关系如图所示,下列结论正确的是( )


| A. | 原混合物中n[Ba(OH)2]:n[NaOH]=1:2 | |
| B. | p点横坐标为120 | |
| C. | p点中溶质为Ba(HCO3)2 | |
| D. | ab段反应可分两段,离子方程式依次为:CO2+2OH-=H2O+CO32- CO2+H2O+CO32-=2HCO3- |
16.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1 molNa2O2中含有的离子总数为4 NA | |
| B. | 0.1 mol羟基(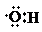 )中含有的电子数为0.7 NA )中含有的电子数为0.7 NA | |
| C. | 室温下,1 L pH=13的NaOH溶液中,水电离出的OH-的数目为0.1 NA | |
| D. | 在5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O中,生成28 g N2时转移的电子数目为3.75 NA |
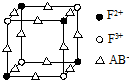 已知A、B、C、D、E、F都是周期表中前 四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子.
已知A、B、C、D、E、F都是周期表中前 四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子.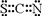 ]-,其中心原子采用sp杂化.
]-,其中心原子采用sp杂化.