题目内容
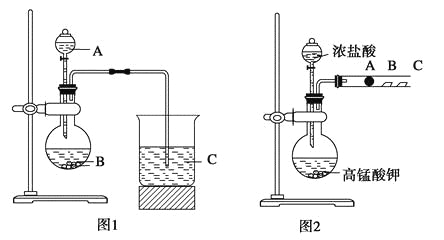
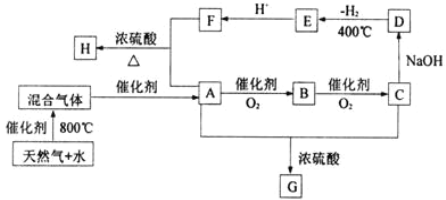
【题目】“C1化学”是指以分子中只含一个碳原子的物质为原料进行物质合成的化学。如下图是以天然气的主要成分为原料的合成路线流程图,其中“混合气体”的成分与水煤气相同;B的水溶液有防腐功能;D是C的钠盐,2 mol D分子间脱去1 mol H2分子可缩合生成E(草酸钠);H是F与A按物质的量之比为1∶2反应的产物。
(1)天然气主要成分的电子式是________;E的化学式是________。
(2)G的结构简式是: _________。
(3)写出下列反应的化学方程式:
A―→B_____________________________;
A+F― →H__________________________。
【答案】(1) ;Na2C2O4;
;Na2C2O4;
(2)HCOOCH3;
(3)2CH3OH+O2![]() 2HCHO+2H2O;HOOC-COOH+2CH3OH
2HCHO+2H2O;HOOC-COOH+2CH3OH![]() CH3OOC-COOCH3
CH3OOC-COOCH3
【解析】
试题分析:天然气与水反应得到“混合物”的主要成分和水煤气的相同,则为CO和H2混合气在催化剂条件下得到A,A经氧化反应得到B,B氧化得到C,那么A为醇,B为醛,C为酸,已知B的水溶液有杀菌防腐能力,则A为甲醇,B为甲醛,C为甲酸,C和氢氧化钠反应生成D为HCOONa,2molD分子间脱去1molH2分子可缩合生成E,E为NaOOC-COONa, H是F与A按物质的量之比为1∶2反应的产物,则H为CH3OOCCOOCH3,A与C反应生成G为HCOOCH3,(1)天然气主要成分的主要成分是甲烷,甲烷的电子式是 ,E是草酸钠,其化学式是Na2C2O4;答案为:
,E是草酸钠,其化学式是Na2C2O4;答案为: ; Na2C2O4;
; Na2C2O4;
(2)G的结构简式为:HCOOCH3,答案为:HCOOCH3;
(3)A到B时甲醇被氧化为甲醛,反应的化学方程式为:2CH3OH+O2![]() 2HCHO+2H2O,A和F生H,即草酸和甲醇生乙二酸二甲酯,反应的化学式为:HOOC-COOH+2CH3OH
2HCHO+2H2O,A和F生H,即草酸和甲醇生乙二酸二甲酯,反应的化学式为:HOOC-COOH+2CH3OH![]() CH3OOC-COOCH3,答案为: 2CH3OH+O2
CH3OOC-COOCH3,答案为: 2CH3OH+O2![]() 2HCHO+2H2O; HOOC-COOH+2CH3OH
2HCHO+2H2O; HOOC-COOH+2CH3OH![]() CH3OOC-COOCH3
CH3OOC-COOCH3

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
T | 最外层电子数是电子层数的3倍 |
Z | 元素最高正价是+7价 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是__________;X的一种氢化物燃烧时火焰温度高,可以焊接金属,则该氢化物的结构式为 ;实验室制取该气体的化学方程式是 。
(2)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为 g。
(3)元素Y与氢元素形成一种离子YH,写出该微粒的电子式____________(用元素符号表示)。实验室检验该微粒的方法是: 。
(4)T元素在周期表的位置: ,其简单阴离子的结构示意图: , 证明该粒子的还原性比Z— 强的离子方程式是 。硒(Se)是人体必需的微量元素,与T在同一主族,Se原子比T原子多一个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物的化学式为________。
(5)元素Z与氢氧化钠溶液反应的化学方程式为 ,其生成的含氧酸盐的电子式为 。
【题目】【加试题】Ⅰ煤化工中常需研究不同温度下平衡常数、投料比等问题。
已知:CO (g)+H2O (g)H2 (g)+CO2 (g)平衡常数K随温度的变化如下表
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题
(1)该反应的平衡常数表达式K= ,△H 0(填“<”、“>”、“=”)
(2)已知在一定温度下,C(s)+CO2 (g)2CO (g)平衡常数K1
C(s)+H2O (g)H2 (g)+CO (g)平衡常数K2,
则K、K1、K2,之间的关系是 。
(3)800℃时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时 间后反应达到平衡,此时CO的转化率为 ;若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40mol CO2,此时v正 v逆 (填“>”、“=”或“<”).