题目内容
下列化学方程式错误的是( )
| A、氯气通入冷的消石灰中 2Cl2+Ca(OH)2═Ca(ClO)2+CaCl2+2H2O |
| B、二氧化氮气体通入氢氧化钠溶液 2NO2+2NaOH═2NaNO3+H2O |
| C、向硫酸铝溶液中滴入氨水 Al2(SO4)3+6NH3?H2O═2Al(OH)3↓+3(NH4)2SO4 |
| D、氧化铝溶解于氢氧化钠溶液 Al2O3+2NaOH═2NaAlO2+H2O |
考点:化学方程式的书写
专题:化学用语专题
分析:A.氯气在碱性条件下自身发生氧化还原反应,可与石灰乳反应生成氯化钙和次氯酸钙;
B.方程式左右氧原子不守恒;
C.向硫酸铝溶液中滴入氨水生成Al(OH)3沉淀,Al(OH)3溶于强酸强碱,不溶于弱酸弱碱;
D.氧化铝为两性氧化物,能够与氢氧化钠溶液反应生成偏铝酸钠和水.
B.方程式左右氧原子不守恒;
C.向硫酸铝溶液中滴入氨水生成Al(OH)3沉淀,Al(OH)3溶于强酸强碱,不溶于弱酸弱碱;
D.氧化铝为两性氧化物,能够与氢氧化钠溶液反应生成偏铝酸钠和水.
解答:
解:A.氯气通人冷的消石灰[Ca(OH)2]中,反应生成CaCl2、Ca(ClO)2、H2O,该反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故A正确;
B.二氧化氮气体通入氢氧化钠溶液,发生反应2NO2+2NaOH=NaNO2+NaNO3+H2O,故B错误;
C. 向硫酸铝溶液中滴入氨水,生成Al(OH)3沉淀,Al(OH)3溶于强酸强碱,氨水呈弱碱性,继续滴加氨水,沉淀Al(OH)3不溶解,反应为Al2(SO4)3+6NH3?H2O═2Al(OH)3↓+3(NH4)2SO4,故C正确;
D.氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O,故D正确;
故选B.
B.二氧化氮气体通入氢氧化钠溶液,发生反应2NO2+2NaOH=NaNO2+NaNO3+H2O,故B错误;
C. 向硫酸铝溶液中滴入氨水,生成Al(OH)3沉淀,Al(OH)3溶于强酸强碱,氨水呈弱碱性,继续滴加氨水,沉淀Al(OH)3不溶解,反应为Al2(SO4)3+6NH3?H2O═2Al(OH)3↓+3(NH4)2SO4,故C正确;
D.氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O,故D正确;
故选B.
点评:本题考查化学反应方程式的书写,为高考高频考点,把握发生的化学反应为解答的关键,注意首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号,题目难度不大.

练习册系列答案
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
某课外实验小组设计的下列实验不合理的是( )
A、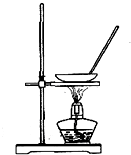 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、 实验室制备少量氨气 |
C、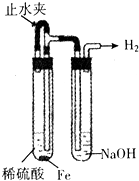 制备并观察氢氧化亚铁 |
D、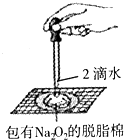 证明过氧化钠与水反应放热 |
在指定的条件下,下列各组离子能大量共存的是( )
| A、使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+ |
| B、强碱性溶液中:K+、Na+、ClO-、S2- |
| C、0.1mol?L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42- |
| D、由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42- |
下列说法正确的是( )
| A、向蒸馏水中滴加浓H2SO4时,KW不变 |
| B、常温下,0.005mol?L-1 Ba(OH)2溶液pH为12 |
| C、Na2CO3水解的离子方程式为:CO32-+2H2O?H2CO3+2OH- |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
下列离子方程式对应的化学方程式正确的是( )
| A、H++OH-═H2O CH3COOH+NaOH═CH3COONa+H2O |
| B、Ba2++SO42-═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O |
| C、CO32-+2H+═CO2↑+H2O CaCO3+2HCl═CaCl2+CO2↑+H2O |
| D、3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O |
有关化学键和化合物的叙述不正确的是( )
| A、盐酸中含有H+和Cl-,所以HCl是离子化合物 |
| B、Na2O2中含有离子键和非极性共价键 |
| C、完全由非金属元素组成的化合物可能是离子化合物 |
| D、双原子或多原子的单质分子中均存在化学键 |
在2A+2B?C+5D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol/(L?s) |
| B、v(B)=0.3 mol/(L?s) |
| C、v(C)=0.4 mol/(L?s) |
| D、v(D)=1 mol/(L?s) |
常温下,0.1mol?L-1 NH4HCO3溶液的pH=7.8,该溶液中微粒浓度间关系正确的是( )
| A、c(OH-)>c(H+) |
| B、c(HCO3-)>c(NH4+) |
| C、c(NH4+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(H2CO3)+c(H+)=c(CO32-)+2c(NH3?H2O)+c(OH-) |