题目内容
在指定的条件下,下列各组离子能大量共存的是( )
| A、使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+ |
| B、强碱性溶液中:K+、Na+、ClO-、S2- |
| C、0.1mol?L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42- |
| D、由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.甲基橙变红的溶液中存在大量的氢离子,Fe2+、Na+、I-、NH4+离子之间不发生反应,也不与氢离子反应;
B.次氯酸根离子具有强氧化性,能够与硫离子发生氧化还原反应;
C.0.1mol?L-1 NaAlO2溶液中,氢离子能够与偏铝酸钠发生反应;
D.H2O电离出的c(H+)=10-11mol/L溶液为酸性或者碱性溶液,碳酸氢根离子既能与酸反应,又能与碱溶液反应.
B.次氯酸根离子具有强氧化性,能够与硫离子发生氧化还原反应;
C.0.1mol?L-1 NaAlO2溶液中,氢离子能够与偏铝酸钠发生反应;
D.H2O电离出的c(H+)=10-11mol/L溶液为酸性或者碱性溶液,碳酸氢根离子既能与酸反应,又能与碱溶液反应.
解答:
解:A.甲基橙变红的溶液为酸性溶液,Fe2+、Na+、I-、NH4+之间不反应,且都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.强碱性溶液中存在大量氢氧根离子,ClO-、S2-之间能够发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.0.1mol?L-1 NaAlO2溶液中,NaAlO2能够与H+发生反应,在溶液中不能大量共存,故C错误;
D.H2O电离出的c(H+)=10-11mol/L溶液中存在大量的氢离子或者氢氧根离子,HCO3-能够与氢氧根离子反应,AlO2-、HCO3-能够与氢离子反应,在溶液中不能大量共存,故D错误;
故选A.
B.强碱性溶液中存在大量氢氧根离子,ClO-、S2-之间能够发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.0.1mol?L-1 NaAlO2溶液中,NaAlO2能够与H+发生反应,在溶液中不能大量共存,故C错误;
D.H2O电离出的c(H+)=10-11mol/L溶液中存在大量的氢离子或者氢氧根离子,HCO3-能够与氢氧根离子反应,AlO2-、HCO3-能够与氢离子反应,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,选项B为易错点,注意次氯酸根离子能够氧化硫离子.

练习册系列答案
相关题目
在冶金工业上,常用电解法得到K、Ca、Na、Mg、Al等金属,其原因是( )
| A、这些金属很活泼 |
| B、都是轻金属 |
| C、这些金属化合物熔点低 |
| D、成本低 |
对元素周期表和元素周期律的发现有突出贡献的科学家是( )
| A、拉瓦锡 | B、门捷列夫 |
| C、阿伏加德罗 | D、道尔顿 |
下列有关太阳能的说法不正确的是( )
| A、太阳能以光波形式传送到地面 |
| B、化石燃料蕴藏的能源来自太阳能 |
| C、太阳能是洁净能源,不污染环境 |
| D、食用植物体内的淀粉、蛋白质等属直接利用能源 |
下列化学方程式错误的是( )
| A、氯气通入冷的消石灰中 2Cl2+Ca(OH)2═Ca(ClO)2+CaCl2+2H2O |
| B、二氧化氮气体通入氢氧化钠溶液 2NO2+2NaOH═2NaNO3+H2O |
| C、向硫酸铝溶液中滴入氨水 Al2(SO4)3+6NH3?H2O═2Al(OH)3↓+3(NH4)2SO4 |
| D、氧化铝溶解于氢氧化钠溶液 Al2O3+2NaOH═2NaAlO2+H2O |
核电荷数小于l8的某元素X,其原子的电子层数为n,最外层电子数为(2n+1),原子核内质子数为(2n2-1).下列关于元素X的说法中不正确的是( )
| A、其最高化合价一定为+5 |
| B、可以形成化学式为KXO3的盐 |
| C、其氢化物可以用来做喷泉实验 |
| D、其最高价氧化物的水化物是强酸 |
下列几组判断均正确的是( )
①
H和
H互为同位素
②O2和O3互为同素异形体
③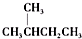 和
和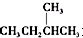 为同分异构体
为同分异构体
④ 和
和 为同一物质
为同一物质
⑤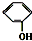 和
和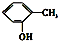 为同系物
为同系物
⑥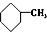 和
和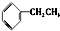 为芳香化合物.
为芳香化合物.
①
1 1 |
2 1 |
②O2和O3互为同素异形体
③
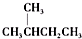 和
和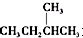 为同分异构体
为同分异构体④
 和
和 为同一物质
为同一物质⑤
 和
和 为同系物
为同系物⑥
 和
和 为芳香化合物.
为芳香化合物.| A、①②④⑤ | B、①③④⑥ |
| C、①②⑤⑥ | D、②③④⑤ |
 如图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
如图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白: