题目内容
某课外实验小组设计的下列实验不合理的是( )
A、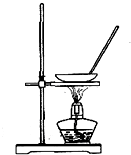 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、 实验室制备少量氨气 |
C、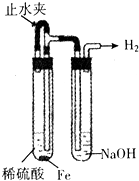 制备并观察氢氧化亚铁 |
D、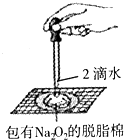 证明过氧化钠与水反应放热 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.NH4Cl受热易分解;
B.CaO与水反应生成氢氧化钙,OH-浓度增大,使NH3+H2O?NH3.H2O?NH4++OH-平衡逆向移动;
C.生成的氢气将装置中的空气排除,关闭止水夹,氢气产生的压强使硫酸亚铁与NaOH接触;
D.过氧化钠与水生成氧气,放出热量,脱脂棉燃烧.
B.CaO与水反应生成氢氧化钙,OH-浓度增大,使NH3+H2O?NH3.H2O?NH4++OH-平衡逆向移动;
C.生成的氢气将装置中的空气排除,关闭止水夹,氢气产生的压强使硫酸亚铁与NaOH接触;
D.过氧化钠与水生成氧气,放出热量,脱脂棉燃烧.
解答:
解:A.NH4Cl受热易分解,不能利用蒸发结晶法得到晶体,应利用冷却结晶法,故A错误;
B.CaO与水反应生成氢氧化钙,OH-浓度增大,使NH3+H2O?NH3.H2O?NH4++OH-平衡逆向移动,则使氨气逸出,可制备氨气,故B正确;
C.生成的氢气将装置中的空气排除,关闭止水夹,氢气产生的压强使硫酸亚铁与NaOH接触,则生成氢氧化亚铁,并保存时间较长,故C正确;
D.过氧化钠与水生成氧气,脱脂棉燃烧,可说明反应放出热量,故D正确;
故选A.
B.CaO与水反应生成氢氧化钙,OH-浓度增大,使NH3+H2O?NH3.H2O?NH4++OH-平衡逆向移动,则使氨气逸出,可制备氨气,故B正确;
C.生成的氢气将装置中的空气排除,关闭止水夹,氢气产生的压强使硫酸亚铁与NaOH接触,则生成氢氧化亚铁,并保存时间较长,故C正确;
D.过氧化钠与水生成氧气,脱脂棉燃烧,可说明反应放出热量,故D正确;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯方法、制备原理、性质等为解答的关键,注意物质制备及性质实验的评价,题目难度不大.

练习册系列答案
相关题目
下列关于有机物的叙述,不正确的是( )
| A、烃分子中,含有的氢原子个数一定是偶数 |
| B、用化学式C4H10表示的物质一定是纯净物 |
C、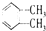 与 与 是同种物质,说明苯分子中碳碳键都相同 是同种物质,说明苯分子中碳碳键都相同 |
| D、某有机物完全燃烧只生成CO2和H2O,则该有机物不一定是烃 |
为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5mL 0.5mol?L-1 KI溶液,滴加0.1mol?L-1 FeCl3溶液5~6滴,充分反应.下列实验操作能验证该反应是否存在限度的是( )
| A、再滴加AgNO3溶液,观察是否有黄色沉淀产生 |
| B、再加入CCl4振荡后,观察下层液体颜色是否变为紫红色 |
| C、再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察有否白色沉淀产生 |
| D、再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变血红色 |
在冶金工业上,常用电解法得到K、Ca、Na、Mg、Al等金属,其原因是( )
| A、这些金属很活泼 |
| B、都是轻金属 |
| C、这些金属化合物熔点低 |
| D、成本低 |
根据下列事实,可知X、Y、Z、W还原性由强到弱的顺序是( )
①X+Y2+=X2++Y
②Z+2H2O
Z(OH)2+H2↑
③Z2+比X2+的氧化性弱
④Y元素最高价氧化物对应水化物的碱性比W元素最高价氧化物对应水化物的碱性强.
①X+Y2+=X2++Y
②Z+2H2O
| ||
③Z2+比X2+的氧化性弱
④Y元素最高价氧化物对应水化物的碱性比W元素最高价氧化物对应水化物的碱性强.
| A、X>Z>Y>W |
| B、Z>W>X>Y |
| C、Z>X>Y>W |
| D、Z>Y>X>W |
下列化学方程式错误的是( )
| A、氯气通入冷的消石灰中 2Cl2+Ca(OH)2═Ca(ClO)2+CaCl2+2H2O |
| B、二氧化氮气体通入氢氧化钠溶液 2NO2+2NaOH═2NaNO3+H2O |
| C、向硫酸铝溶液中滴入氨水 Al2(SO4)3+6NH3?H2O═2Al(OH)3↓+3(NH4)2SO4 |
| D、氧化铝溶解于氢氧化钠溶液 Al2O3+2NaOH═2NaAlO2+H2O |
 如图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
如图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白: