题目内容
5.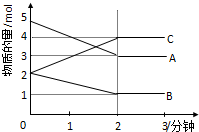 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.(1)则该反应的反应物A、B,生成物是C,化学方程式为2A+B?2C;
(2)能否计算反应开始至2分钟时,用C表示的反应速率?若能,其反应速率为不能,
若不能,则其原因为因为缺少体积;
(3)2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了化学平衡状态.
分析 (1)从物质的物质的量的变化趋势判断反应物和生成物,根据物质的物质的量变化值等于化学计量数之比书写化学方程;
(2)化学反应速率是单位时间内浓度的变化;
(3)当反应达到平衡状态时,各物质的物质的量不再变化.
解答 解:(1)由图象可以看出,A、B的物质的量逐渐减小,则A、B为反应物,C的物质的量逐渐增多,作为C为生成物,
当反应到达2min时,△n(A)=2mol,△n(B)=1mol,△n(C)=2mol,
化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=2:1:2,
所以反应的化学方程式为:2A+B?2C,
故答案为:A、B; C; 2A+B?2C;
(2)由于不能确定溶液的体积,则不能计算浓度的变化,无法计算反应速率,故答案为:不能,因为缺少体积;
(3)当反应达到平衡状态时,各物质的物质的量不再变化,2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了平衡状态,故答案为:化学平衡.
点评 本题考查化学平衡图象问题,题目难度不大,注意把握由图象判断化学方程式的方法.

练习册系列答案
相关题目
15.将10moLA和5moLB放入10L真空容器中,某温度下发生反应:3A(g)+B(g)?2C(g),在最初的0•2秒内,A的平均速率为0•06moL/(L•s),则在0.2秒时,容器中C的物质的量为( )
| A. | 0•12mol | B. | 0•08mol | C. | 0•04mol | D. | 0•8mol |
16.相同质量的下列物质与足量盐酸反应,产生CO2最少的是( )
| A. | Na2CO3 | B. | NaHC03 | C. | K2CO3 | D. | CaCO3 |
17.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 60 g SiO2晶体中含有Si-O键数目为2NA | |
| B. | 常温常压下,1.6 9 O2和O3的混合气体所含电子数为0.8NA | |
| C. | 1 mol/L AICl3溶液中,所含Al3+数目小于NA | |
| D. | 密闭容器中2 mol NO与l mol 02充分反应,产物的分子数为2NA |

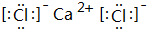 ;
;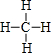 .
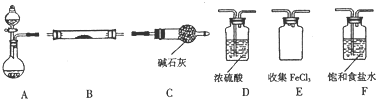
.
 .
.