题目内容
14.某研究性学习小组就Na2O2的有关性质探究如下:向滴有酚酞的水中投入一定量的Na2O2,观察到先有大量气泡产生,溶液变红,过一会儿溶液又变为无色,对上述实验中溶液变红,过一会儿又褪色的原因,甲、乙两同学提出了不同的解释:甲同学认为是Na2O2与水反应放出氧气,氧气有氧化性,将酚酞氧化而使溶液褪色;
乙同学则认为是Na2O2与水反应时产生了H2O2,H2O2的强氧化性使酚酞褪色.
(1)写出Na2O2与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑;
(2)乙同学设计了如下实验来证明白己的猜想是正确的:在滴有酚酞的氢氧化钠溶液中滴加3%的H2O2溶液并振荡.
①若乙同学的猜想正确,可观察到的现象是溶液的红色褪去;
②甲同学针对乙同学的上述实验提出还应增做实验才能更直接证明Na2O2与水反应生成了H2O2,甲同学提出要增加的实验是什么?在滴有酚酞的水中加入足量过氧化钠,待反应完成后向溶液中加入少量二氧化锰粉末,有气体放出,证明过氧化钠与水反应时有H2O2生成
(3)试设计简单实验证明甲同学解释是否正确(画出简易装置图).
分析 (1)过氧化钠与水反应生成氢氧化钠和氧气;
(2)依据H2O2有漂白性,能漂白酚酞解答;
②H2O2在MnO2催化下能放出氧气,可在加入过氧化钠后的水溶液中加入少量MnO2,有气泡放出可直接证明过氧化钠与水反应有H2O2生成;
(3)要验证是氧气氧化酚酞,则可向滴有酚酞水中直接通入氧气来检验.
解答 解:(1)过氧化钠与水反应生成氢氧化钠和氧气,化学方程式:2Na2O2+2H2O=4NaOH+O2↑;
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(2)①双氧水具有漂白性,能够漂白红色的酚酞溶液
故答案为:溶液的红色褪去;
②H2O2在MnO2催化下能放出氧气,可在加入过氧化钠后的水溶液中加入少量MnO2,有气泡放出可直接证明过氧化钠与水反应有H2O2生成;
故答案为:在滴有酚酞的水中加入足量过氧化钠,待反应完成后向溶液中加入少量二氧化锰粉末,有气体放出,证明过氧化钠与水反应时有H2O2生成;
(3))向滴有酚酞的氢氧化钠溶液中通入氧气,若红色褪去,证明甲同学的推测正确,反之,则不正确,装置图为: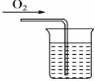 ,
,
故答案为: .
.
点评 本题为实验探究,考查了过氧化钠与氧气的反应,明确反应实质是解题关键,注意实验设计合理性,题难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
4.区分下列各组物质,所用的两种方法不完全正确的一组是( )
| 选项 | 需区分的物质 | 区分方法 |
| A | 蒸馏水和自来水 | ①蒸发 ②看颜色 |
| B | 食盐和面碱(Na2CO3) | ①加食醋 ②测其溶液酸碱性 |
| C | 小苏打和碳酸氢氨 | ①灼烧 ②做焰色反应 |
| D | 黑醋和酱油 | ①闻气味 ②尝味道 |
| A. | A | B. | B | C. | C | D. | D |
2. 如图所示的电化学装置,可用于净化处理厕所排放废水中的尿素( H2 NCON H2),同时产生电能.下列有关说法不正确的是( )
如图所示的电化学装置,可用于净化处理厕所排放废水中的尿素( H2 NCON H2),同时产生电能.下列有关说法不正确的是( )
 如图所示的电化学装置,可用于净化处理厕所排放废水中的尿素( H2 NCON H2),同时产生电能.下列有关说法不正确的是( )
如图所示的电化学装置,可用于净化处理厕所排放废水中的尿素( H2 NCON H2),同时产生电能.下列有关说法不正确的是( )| A. | 右侧的多孔碳电极是原电池的负极 | |
| B. | 电解质溶液中H十向左侧移动 | |
| C. | 正极上发生还原反应:H2NCONH2+H2O-6e-═c-CO2+N2+6N+ | |
| D. | 电极上消耗标准状况下33.6LO2,电路中转移6 mol电子 |
9.在体积相同的两个密闭容器中分别充满A、B气体,当这两个容器内温度相等时,下列说法正确的是( )
| A. | 若A为O2,B为O3,它们质量相等时则容器中氧原子个数不相等 | |
| B. | 若A为NO2,B为N2O4,它们压强相等时则质量相等 | |
| C. | 若A为C2H4,B为C2H6,它们密度相等时则气体的物质的量相等 | |
| D. | 若A为CO2,B为C3H8,它们密度相等时则分子数相等 |
19.对一定量气体体积的探究.
已知1 mol不同气体在不同条件下的体积.
(1)从上表分析得出的结论:①1 mol任何气体在标准状况下的体积都约为22.4L.
②1 mol不同的气体,在不同的条件下,体积不一定(填“一定”、“一定不”或“不一定”)相等.
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:①分子大小相同,②分子间距相同.
(3)应用:在标准状况下,48g O3的体积为多少升?(写出计算过程)
已知1 mol不同气体在不同条件下的体积.
| 化学式 | 条件 | 1mol气体体积 |
| H2 | 0℃,101kPa | 22.4 |
| O2 | 0℃,101kPa | 22.4 |
| CO | 0℃,101kPa | 22.4 |
| H2 | 0℃,202kPa | 11.2 |
| CO2 | 0℃,202kPa | 11.2 |
| N2 | 273℃,202kPa | 22.4 |
| NH3 | 273℃,202kPa | 22.4 |
②1 mol不同的气体,在不同的条件下,体积不一定(填“一定”、“一定不”或“不一定”)相等.
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:①分子大小相同,②分子间距相同.
(3)应用:在标准状况下,48g O3的体积为多少升?(写出计算过程)
19.下列有关实验能达到目的是( )
| A. |  装置:除去Cl2中的HCl杂质 装置:除去Cl2中的HCl杂质 | |
| B. | 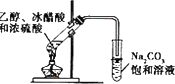 装置:制取乙酸乙酯 装置:制取乙酸乙酯 | |
| C. | 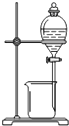 装置:用酒精萃取碘水中的碘单质 装置:用酒精萃取碘水中的碘单质 | |
| D. |  烧瓶中充满氨气,烧杯中盛装四氯化碳,可产生喷泉现象 烧瓶中充满氨气,烧杯中盛装四氯化碳,可产生喷泉现象 |
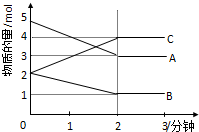 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.