题目内容
2.92gNaHCO3和KHCO3的混合物和足量的盐酸反应,收集到标准状况下二氧化碳气体22.4L,求混合物中NaHCO3、KHCO3的物质的量.分析 二者与足量稀盐酸反应生成二氧化碳,n(CO2)=$\frac{22.4L}{22.4L/mol}$=1mol,根据C原子守恒得n(CO2)=n(NaHCO3)+n(KHCO3)=1mol,设NaHCO3的物质的量为xmol,则KHCO3的物质的量是(1-x)mol,根据混合物质量计算二者物质的量.
解答 解:二者与足量稀盐酸反应生成二氧化碳,n(CO2)=$\frac{22.4L}{22.4L/mol}$=1mol,根据C原子守恒得n(CO2)=n(NaHCO3)+n(KHCO3)=1mol,设NaHCO3的物质的量为xmol,则KHCO3的物质的量是(1-x)mol,
混合物质量=84xg+100(1-x)g=92g,x=0.5,则碳酸氢钾的物质的量=1mol-0.5mol=0.5mol,
答:混合物中NaHCO3、KHCO3的物质的量都是0.5mol.
点评 本题考查混合物的有关计算,为高频考点,侧重考查学生分析计算能力,利用原子守恒分析解答即可,题目难度不大.

练习册系列答案
相关题目
12.在2L 0.5mol/L 的Na2SO4溶液中,含有Na+( )
| A. | 0.5mol | B. | 1mol | C. | 2mol | D. | 23g |
13.NA为阿伏加德罗常数的值,下列物质所含粒子数为0.2NA的是( )
| A. | 标准状况下,2.24 LCl2中含有的共价键数 | |
| B. | 100g质量分数为16.2%HBr溶液中的氢原子数 | |
| C. | 3.9g Na202晶体中所含的离子总数 | |
| D. | 0.1mol H2S和0.1 mol SO2混合后,体系中的硫原子数 |
17.在某温度下,将1mol A和2mol B充入一密闭容器中,发生反应:aA(g)+B(g)?C(g)+D(g),一段时间后达平衡,已知各物质的平衡浓度的关系为ca(A)•c(B)=c(C)•c(D).若温度不变,将容器的体积缩小为原来的$\frac{1}{2}$,A 的转化率没有发生变化,则B的转化率为( )
| A. | 60% | B. | 40% | C. | 33.3% | D. | 66.7% |
7.超级储能可充电氟镁动力电池性能比电池优良,其工作原理如图所示,电池总反应为Mg+2MnF3═2MnF2+MgF2.下列有关说法正确的是( )
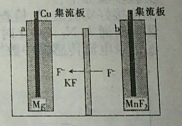

| A. | b为负极 | |
| B. | 该电池放电时,Cu集流板上Cu失电子 | |
| C. | 充电时,F-通过交换膜从b极区移向a极区 | |
| D. | 充电时,阳极的电极反应式为2MnF2+2F--2e-═2MnF3 |
14.精炼铜的过程中,电解质溶液中的[Fe2+]、[Zn2+]会逐渐增大而影响进一步电解. 甲同学设计下图除杂方案:
已知:
请回答下列问题:

(1)加入H2O2目的是将Fe2+氧化为Fe3+.
(2)乙同学认为应将方案中的pH调节至8,你认为此观点不正确(填“正确”或“不正确”)理由是同时会使Cu2+生成沉淀而除去.
(3)利用铜棒、石墨棒和溶液C(填“B”或“C”)可设计一个原电池.该原电池的正极反应式为Fe3++e-=Fe2+.请在下图中完成该原电池的设计(标出电解质溶液和电子流动方向).

已知:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |

(1)加入H2O2目的是将Fe2+氧化为Fe3+.
(2)乙同学认为应将方案中的pH调节至8,你认为此观点不正确(填“正确”或“不正确”)理由是同时会使Cu2+生成沉淀而除去.
(3)利用铜棒、石墨棒和溶液C(填“B”或“C”)可设计一个原电池.该原电池的正极反应式为Fe3++e-=Fe2+.请在下图中完成该原电池的设计(标出电解质溶液和电子流动方向).

11.取两份等质量的铝份和铁粉,分别与足量的盐酸反应,在相同状态下产生的气体体积之比是( )
| A. | 1:1 | B. | 3:2 | C. | 28:9 | D. | 2:3 |
7.FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S.
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水 FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
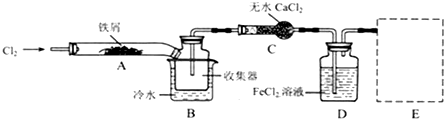
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(2)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)②⑤.
(3)如果没有装置C的设计,会导致D装置中水挥发到接受器,使FeCl3潮解.
(4)用离子方程式表示虚线框E中所增加装置和试剂的作用: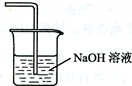 、Cl2+2OH-=Cl-+ClO-+H2O.
、Cl2+2OH-=Cl-+ClO-+H2O.
(5)用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,请写出反应的离子方程式:2Fe3++2H2S=2Fe2++2H++S↓.
Ⅱ.反应结束后,将收集器中所得固体完全溶于稀盐酸,小组同学对所得溶液金属阳离子的成分有三种观点:①只有Fe3+;②只有Fe2+;③既有Fe3+又有Fe2+.
为探究溶液的组成,实验如下:
综合上述实验分析,所得溶液中含有的金属阳离子有Fe3+、Fe2+.
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水 FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:

①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(2)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)②⑤.
(3)如果没有装置C的设计,会导致D装置中水挥发到接受器,使FeCl3潮解.
(4)用离子方程式表示虚线框E中所增加装置和试剂的作用:
 、Cl2+2OH-=Cl-+ClO-+H2O.
、Cl2+2OH-=Cl-+ClO-+H2O.(5)用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,请写出反应的离子方程式:2Fe3++2H2S=2Fe2++2H++S↓.
Ⅱ.反应结束后,将收集器中所得固体完全溶于稀盐酸,小组同学对所得溶液金属阳离子的成分有三种观点:①只有Fe3+;②只有Fe2+;③既有Fe3+又有Fe2+.
为探究溶液的组成,实验如下:
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| ①取少量所得溶液于试管中,加入少量KSCN溶液. | 溶液中出现红色. | 说明:假设②不成立,假设①或③成立; 反应的离子方程式是Fe3++3SCN-=Fe(SCN)3. |
| ②另取少量所得溶液于试管中,加入少量酸性 KMnO4溶液. | 溶液紫红色退去 | 说明:假设②或③成立. |
 某化学兴趣小组的同学为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,他们开展了如下探究性学习.
某化学兴趣小组的同学为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,他们开展了如下探究性学习.