题目内容
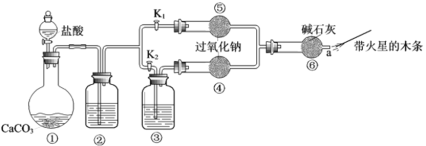
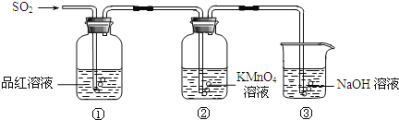
【题目】某研究小组的同学利用如图所示装置探究二氧化硫气体的性质。请回答:
(1)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是____。
(2)当观察到②中溶液颜色变浅时,①中的现象是____。
(3)装置③的作用是___。
(4)①中的现象说明二氧化硫具有的性质是___。
(5)②中的现象说明二氧化硫具有的性质是___。
【答案】Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑ 品红溶液褪色(或变浅) 吸收未反应的二氧化硫,防止污染环境 漂白性 还原性
CuSO4+2H2O+SO2↑ 品红溶液褪色(或变浅) 吸收未反应的二氧化硫,防止污染环境 漂白性 还原性
【解析】
铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫气体和水,二氧化硫具有漂白性,能够使品红溶液褪色反应,二氧化硫有还原性,能使酸性高锰酸钾溶液褪色,二氧化硫有毒,不能直接排放,需要用氢氧化钠溶液吸收。
(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑,故答案为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,故答案为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;
CuSO4+2H2O+SO2↑;
(2)二氧化硫具有漂白性,将二氧化硫通入品红溶液后,会观察到①中品红溶液褪色(或变浅),故答案为:品红溶液褪色(或变浅);
(3)二氧化硫为有毒气体,多余的二氧化硫不能直接排放,所以装置③中氢氧化钠溶液的作用是吸收未反应的SO2,防止污染环境,故答案为:吸收未反应的SO2,防止污染环境;
(4)二氧化硫具有漂白性,能使品红溶液褪色,装置①中品红溶液褪色,证明二氧化硫具有漂白性,故答案为:漂白性;
(5)二氧化硫具有还原性,酸性高锰酸钾溶液具有强氧化性,二氧化硫能使酸性高锰酸钾溶液褪色,②中酸性高锰酸钾溶液褪色,说明二氧化硫具有还原性,故答案为:还原性。

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案
相关题目