题目内容
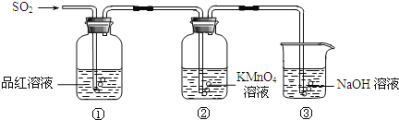
【题目】在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
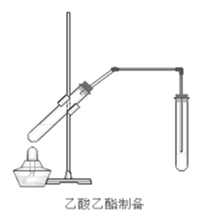
(1)写出制取乙酸乙酯的化学反应方程式________
(2)浓硫酸的作用是:①________;②________。
(3)饱和碳酸钠溶液的主要作用是________、________、________。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中的目的是防止________。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是________。
(6)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是________。
【答案】CH3CHOOH+C2H5OH→CH3COOC2H5+H2O 催化剂 吸水剂 除去乙酸 吸收乙醇 降低乙酸乙酯的溶解度,便于析出 倒吸 分液 防止暴沸
【解析】
在浓硫酸做催化剂和吸收剂作用下,乙酸和乙醇共热发生酯化反应生成乙酸乙酯和水,酯化反应是可逆反应,反应中浓硫酸除了起到催化剂的作用外,还起到吸水剂的作用,实验时应加入几块碎瓷片起到防止暴沸的作用,乙酸乙酯中混有乙醇和乙酸,乙酸乙酯不溶于水,乙醇能与水互溶,乙酸具有酸性,能与碳酸钠溶液反应,饱和碳酸钠溶液的主要作用是降低乙酸乙酯的溶解度,便于分层、溶解乙醇杂质、除去乙酸杂质,导管插在饱和碳酸钠溶液的液面下可能发生倒吸,通蒸气的导管要插在饱和碳酸钠溶液的液面上,用分液的方法制得的乙酸乙酯分离出来。
(1)在浓硫酸做催化剂和吸收剂作用下,乙酸和乙醇共热发生酯化反应生成乙酸乙酯和水,反应的化学方程式为CH3CHOOH+C2H5OH![]() CH3COOC2H5+H2O,故答案为:CH3CHOOH+C2H5OH
CH3COOC2H5+H2O,故答案为:CH3CHOOH+C2H5OH![]() CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(2)酯化反应是可逆反应,反应中浓硫酸除了起到催化剂的作用外,还起到吸水剂的作用,使平衡向正反应方向移动,有利于乙酸乙酯的生成,故答案为:催化剂;吸水剂;
(3)乙酸乙酯不溶于水,乙醇能与水互溶,乙酸具有酸性,能与碳酸钠溶液反应,乙酸乙酯中混有乙醇和乙酸,则右边试管内所盛饱和碳酸钠溶液的主要作用是降低乙酸乙酯的溶解度,便于分层、溶解乙醇杂质、除去乙酸杂质,故答案为:除去乙酸;溶解乙醇;降低乙酸乙酯的溶解度,便于析出;
(4)导管不能插入溶液中是因为利用饱和碳酸钠溶液中和挥发出来的乙酸,导管插在饱和碳酸钠溶液的液面下可能发生倒吸,故答案为:防止倒吸;
(5)若要把制得的乙酸乙酯分离出来,应先将盛有混合物的试管充分振荡,使乙酸、乙醇溶解,静置分层后取上层得乙酸乙酯,故答案为:分液;
(6)在给混合液体加热时,加入碎瓷片可以防止暴沸,由于酯化反应的反应物都是液态,所以实验时应加入几块碎瓷片起到防止暴沸的作用,故答案为:防止暴沸。

【题目】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
溶质的质量分数 | 溶液的密度(g·cm-3) | |
第一份溶液 | w1 | ρ1 |
第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___w4;若ρ1<ρ2,w3______w4(填“>”“<”或“=”)。