题目内容
【题目】(1)某温度(T℃)时,水的Kw=1×10-12,则该温度___(填“>”、“<”或“=”)25℃,其理由是___。
(2)该温度下,c(H+)=1×10-7mol·L-1的溶液呈___(填“酸性”、“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=____mol·L-1。
【答案】> 升温促进水电离,Kw增大 碱性 1×10-7
【解析】
(1)电离吸热,升高温度,促进水电离;(2)根据c(OH-)、c(H+)的相对大小判断溶液酸碱性;
NaOH抑制水电离;
(1)25℃,Kw=1×10-14;升高温度,Kw增大,现Kw=1×10-12>1×10-14,因此温度大于25 ℃。
(2)该温度下c(H+)=1×10-7mol·L-1,该溶液中c(OH-)=![]() mol·L-1=1×10-5mol·L-1>c(H+),溶液呈碱性。
mol·L-1=1×10-5mol·L-1>c(H+),溶液呈碱性。
无论什么溶液,水电离的c(H+)和水电离c(OH-)永远相等,则c(H+)水=c(OH-)水。在碱的溶液中,溶液中OH-来自于水和碱的电离,溶液中H+只来源于水电离,用溶液中H+衡量水的电离,c(OH-)水=1×10-7mol·L-1。

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
【题目】下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
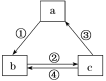
选项 | a | b | c | 箭头上所标数字的反应条件 |
A | AlCl3 | NaAlO2 | Al(OH)3 | ①加入过量的NaOH |
B | Si | SiO2 | H2SiO3 | ②常温加水 |
C | NaOH | NaHCO3 | Na2CO3 | ③加澄清石灰水 |
D | Fe | FeCl3 | FeCl2 | ④加入氯气 |
A.AB.BC.CD.D
