题目内容
【题目】中国环境监测总站数据显示,颗粒物![]() 等
等![]() 为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对
为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对![]() 、
、![]() 、
、![]() 等进行研究具有重要意义。请回答下列问题:
等进行研究具有重要意义。请回答下列问题:
(1)将![]() 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 |
|
|
|
|
|
|
浓度 |
|
|
|
|
|
|
根据表中数据计算![]() 待测试样的pH =___________。
待测试样的pH =___________。
(2)汽车发动机工作时会引发![]() 和
和![]() 反应,当尾气中空气不足时,
反应,当尾气中空气不足时,![]() 在催化转化器中被还原成
在催化转化器中被还原成![]() 排出。写出NO被CO还原的化学方程式________。
排出。写出NO被CO还原的化学方程式________。
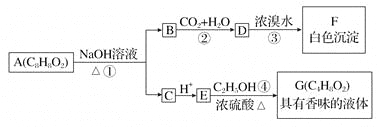
(3)碘循环工艺不仅能吸收![]() 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应_______。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出![]() 的目的是_______。
的目的是_______。
(4)下图是用![]() 脱除烟气中NO的原理。
脱除烟气中NO的原理。
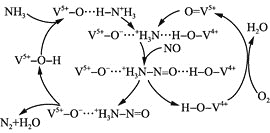
①该脱硝原理中,NO最终转化为 ________![]() 填化学式
填化学式![]() 和H2O。
和H2O。
②当消耗![]() 和
和![]() 时,除去的NO在标准状况下的体积为____L。
时,除去的NO在标准状况下的体积为____L。
【答案】4 ![]()
![]()
![]() 分解为可逆反应,及时分离出产物
分解为可逆反应,及时分离出产物![]() ,有利于反应正向进行
,有利于反应正向进行 ![]() 44.8
44.8
【解析】
![]() 由溶液中电荷守恒进行计算;
由溶液中电荷守恒进行计算;
![]() 在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:
在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:![]() ;
;
![]() 从流程图可知,在反应器中,
从流程图可知,在反应器中,![]() 氧化
氧化![]() ,生成硫酸和HI;
,生成硫酸和HI;
![]() 由题意可知,在HI分解反应中使用膜反应器分离出
由题意可知,在HI分解反应中使用膜反应器分离出![]() 的目的是HI分解为可逆反应,及时分离出产物
的目的是HI分解为可逆反应,及时分离出产物![]() ,有利于反应正向进行;
,有利于反应正向进行;
![]() 根据脱硝原理图,可知NO最终转化为
根据脱硝原理图,可知NO最终转化为![]() ;
;
![]() 、
、![]() 、
、![]() 三者共同反应,生成
三者共同反应,生成![]() 和
和![]() 。
。
![]() 由溶液中电荷守恒:
由溶液中电荷守恒:![]() ,得
,得![]() ,pH值为4;
,pH值为4;
![]() 在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:
在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:;
![]() 从流程图可知,在反应器中,
从流程图可知,在反应器中,![]() 氧化
氧化![]() ,生成硫酸和HI,反应方程式为:
,生成硫酸和HI,反应方程式为:![]() ;
;
![]() 由题意可知,在HI分解反应中使用膜反应器分离出
由题意可知,在HI分解反应中使用膜反应器分离出![]() 的目的是HI分解为可逆反应,及时分离出产物
的目的是HI分解为可逆反应,及时分离出产物![]() ,有利于反应正向进行;
,有利于反应正向进行;
![]() 根据脱硝原理图,可知NO最终转化为
根据脱硝原理图,可知NO最终转化为![]() ;
;
![]() 、
、![]() 、
、![]() 三者共同反应,生成
三者共同反应,生成![]() 和
和![]() 。当消耗
。当消耗![]() 时,失去电子的物质的量为6mol;
时,失去电子的物质的量为6mol;![]() ,得到电子的物质的量为2mol,所以NO得到电子的物质的量为4mol,所以消耗NO的物质的量为2mol,体积为
,得到电子的物质的量为2mol,所以NO得到电子的物质的量为4mol,所以消耗NO的物质的量为2mol,体积为![]() 。
。

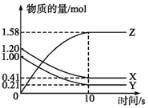
【题目】在一体积2L的密闭容器中加入反应物N2、H2,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
物质的量/ mol 时间/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0~2 min内,NH3的反应速率为0.1 mol·Lˉ1·minˉ1
B. 2 min时, H2的物质的量0.3 mol
C. 4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D. 4~6 min内,容器内气体分子的总物质的量不变