题目内容
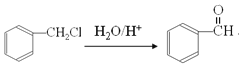
【题目】利用下述操作步骤:①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入过量![]() 生成
生成![]() 沉淀 ⑤加盐酸生成
沉淀 ⑤加盐酸生成![]() 沉淀,由含少量铁粉的铝粉制取纯净的氢氧化铝,最恰当的组合是( )
沉淀,由含少量铁粉的铝粉制取纯净的氢氧化铝,最恰当的组合是( )
A.②③④③B.②③⑤③C.①③④③D.②⑤③④
【答案】A
【解析】
含少量铁粉的铝粉中若先加盐酸,两种金属都溶解,生成FeCl2、AlCl3,再加过量的碱,FeCl2转化为Fe(OH)2,继而转化为Fe(OH)3,AlCl3转化为NaAlO2,过滤出Fe(OH)3,得NaAlO2溶液,再通入过量CO2,再过滤才能得到Al(OH)3,此操作共需五个步骤,且Fe(OH3是胶状沉淀,过滤起来比较困难,所以应采用先加NaOH溶液溶解。
加烧碱溶液(②)溶解,得到NaAlO2溶液和Fe,过滤(③)得NaAlO2溶液,再通入过量![]() 生成
生成![]() 沉淀(④),最后再过滤(③),即得纯净的氢氧化铝。
沉淀(④),最后再过滤(③),即得纯净的氢氧化铝。
所以操作顺序为②③④③。
答案为A。

【题目】中国环境监测总站数据显示,颗粒物![]() 等
等![]() 为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对
为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对![]() 、
、![]() 、
、![]() 等进行研究具有重要意义。请回答下列问题:
等进行研究具有重要意义。请回答下列问题:
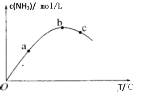
(1)将![]() 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 |
|
|
|
|
|
|
浓度 |
|
|
|
|
|
|
根据表中数据计算![]() 待测试样的pH =___________。
待测试样的pH =___________。
(2)汽车发动机工作时会引发![]() 和
和![]() 反应,当尾气中空气不足时,
反应,当尾气中空气不足时,![]() 在催化转化器中被还原成
在催化转化器中被还原成![]() 排出。写出NO被CO还原的化学方程式________。
排出。写出NO被CO还原的化学方程式________。
(3)碘循环工艺不仅能吸收![]() 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应_______。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出![]() 的目的是_______。
的目的是_______。
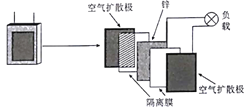
(4)下图是用![]() 脱除烟气中NO的原理。
脱除烟气中NO的原理。
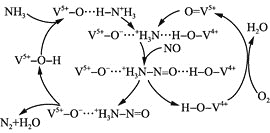
①该脱硝原理中,NO最终转化为 ________![]() 填化学式
填化学式![]() 和H2O。
和H2O。
②当消耗![]() 和
和![]() 时,除去的NO在标准状况下的体积为____L。
时,除去的NO在标准状况下的体积为____L。
【题目】A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复)。
阳离子 | Na+、Ba2+、NH4+ |
阴离子 | CH3COO-、Cl-、OH-、SO42- |
已知:①A、C溶液的pH均大于7,相同浓度A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A是___,B是___。
(2)写出C与D反应的离子方程式___。
(3)25℃时,0.1mol·L-1B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)=___(用含有a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为___。
(5)在一定体积的0.005mol·L-1的C溶液中,加入一定体积的0.00125mol·L-1的盐酸时,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是___。