题目内容
【题目】下列反应中,氧化剂和还原剂的物质的量之比最大的是( )
A. 氯气和氨气 3Cl2 + 8NH3 = N2 + 6NH4Cl
B. 铜和稀硝酸3Cu + 8HNO3(稀) = 2NO↑+ 3Cu(NO3)2 + 4H2O
C. 氢气和氧化铁 3H2 + Fe2O3![]() 2Fe + 3H2O
2Fe + 3H2O
D. 二氧化锰和盐酸 MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
【答案】A
【解析】A. 氯气和氨气 3Cl2 + 8NH3 = N2 + 6NH4Cl,Cl2 中元素化合价降低是氧化剂,NH3中元素化合价升高是还原剂,氧化剂和还原剂的物质的量之比3:2;B. 铜和稀硝酸3Cu + 8HNO3(稀) = 2NO↑+ 3Cu(NO3)2 + 4H2O,HNO3中元素化合价降低是氧化剂,Cu中元素化合价升高是还原剂,氧化剂和还原剂的物质的量之比2:3;C. 氢气和氧化铁 3H2 + Fe2O3![]() 2Fe + 3H2O,Fe2O3中元素化合价降低是氧化剂,H2 中元素化合价升高是还原剂,氧化剂和还原剂的物质的量之比1:3;D. 二氧化锰和盐酸 MnO2 + 4HCl(浓)
2Fe + 3H2O,Fe2O3中元素化合价降低是氧化剂,H2 中元素化合价升高是还原剂,氧化剂和还原剂的物质的量之比1:3;D. 二氧化锰和盐酸 MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑+ 2H2O, MnO2中元素 化合价降低是氧化剂,HCl中元素化合价升高是还原剂,氧化剂和还原剂的物质的量之比1:2;综上所述,选A。
MnCl2 + Cl2↑+ 2H2O, MnO2中元素 化合价降低是氧化剂,HCl中元素化合价升高是还原剂,氧化剂和还原剂的物质的量之比1:2;综上所述,选A。

 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案【题目】某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3溶液的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
实验编号 | T(K) | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
① | 298 | 粗颗粒 | 2.00 | (I)实验①和②探究HNO3浓度对该反应速率的影响 (II)实验①和____探究温度对该反应速率的影响; (III)实验①和____探究大理石规格(粗、细)对该反应速率的影响。 |
② | _____ | _______ | __________ | |
③ | _____ | _______ | __________ | |
④ | _____ | _______ | __________ |
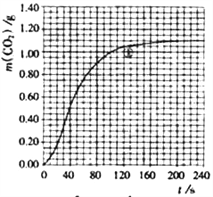
(2)实验①中CO2质量随时间变化的关系见下图:依据反应方程式![]() CaCO3+HNO3=
CaCO3+HNO3=![]() Ca(NO3)2+
Ca(NO3)2+![]() CO2↑+
CO2↑+![]() H2O,计算实验①在70-90 s范围内HNO3的平均反应速率____________,写出计算过程[忽略溶液体积变化,且70s时m(CO2)=0.84g,90s时m(CO2)=0.95g]。
H2O,计算实验①在70-90 s范围内HNO3的平均反应速率____________,写出计算过程[忽略溶液体积变化,且70s时m(CO2)=0.84g,90s时m(CO2)=0.95g]。
【题目】在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:A(g)![]() B(g)+C(g) △H =+85.1kJ/mol 反应时间(t)与容器内总压强(P)的数据见下表:
B(g)+C(g) △H =+85.1kJ/mol 反应时间(t)与容器内总压强(P)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强P/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
计算平衡时A的转化率__________和平衡常数___________________。