题目内容
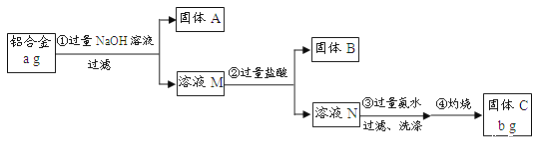
【题目】三氯化六氨合钴[Co(NH3)6]Cl3是橙黄色的配合物,是合成其它一些含钴配合物的原料。利用含钴废料(含少量Fe、Al等杂质)制取[Co(NH3)6]Cl3的工艺流程如图,回答下列问题:
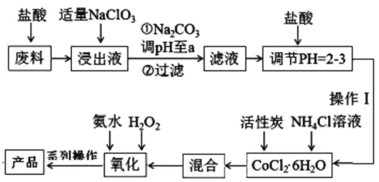
已知:①“浸出液”中含有Co2+、Fe2+、Fe3+、Al3+等
②Ksp[Co(OH)2]=6×10-15、Ksp[Co(OH)3]=1.6×10-44
(1)加“适量NaClO3”的作用是___,发生反应的离子方程式为___。
(2)“加Na2CO3调pH至a”会生成两种沉淀,分别为___(填化学式)。
(3)操作Ⅰ的步骤包括___、___、减压过滤。
(4)流程中“氧化”过程应先加入___(填“氨水”或“H2O2”),需水浴控温在50~60℃,温度不能过高,原因是___。写出“氧化”步骤发生反应的离子方程式:___,若无活性炭作催化剂,所得固体产物中除[Co(NH3)6]Cl3外还会有大量二氯化一氯五氨合钴[Co(NH3)5Cl]Cl2和三氯化五氨一水合钴[Co(NH3)5H2O]Cl3晶体,这体现了催化剂的___性。
【答案】将Fe2+转化为Fe3+ 6Fe2++ClO![]() +6H+=6Fe3++Cl-+3H2O Fe(OH)3和Al(OH)3 蒸发浓缩 冷却结晶 氨水 氨水温度过高会导致H2O2大量分解,降低产率 H2O2+2Co2++2NH
+6H+=6Fe3++Cl-+3H2O Fe(OH)3和Al(OH)3 蒸发浓缩 冷却结晶 氨水 氨水温度过高会导致H2O2大量分解,降低产率 H2O2+2Co2++2NH![]() +10NH3·H2O+6Cl-=2[Co(NH3)6]Cl3↓+12H2O 选择性
+10NH3·H2O+6Cl-=2[Co(NH3)6]Cl3↓+12H2O 选择性
【解析】
以含钴废料(含少量Fe、Al等杂质)制取[Co(NH3)6]Cl3:用盐酸溶解废料,得到Co2+、Fe2+、Al3+的酸性溶液,加入适量的NaClO3将Fe2+氧化为Fe3+,再加Na2CO3调pH,沉淀Al3+、Fe3+为Fe(OH)3和Al(OH)3,过滤,得到滤液,向含有Co2+的溶液中加入盐酸调节pH=2-3,加入活性炭和NH4Cl溶液得到CoCl26H2O,再依次加入氨水和H2O2,发生反应:H2O2+2CoCl2+2NH4Cl+10NH3H2O=2[Co(NH3)6]Cl3↓+12H2O,再将沉淀在HCl氛围下蒸发浓缩、冷却结晶、减压过滤得到产品,据此分析作答。
(1)加“适量NaClO3”的目的是将Fe2+氧化为Fe3+,发生的离子反应为:6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O;
(2)根据分析,加Na2CO3调pH,沉淀Al3+、Fe3+为Fe(OH)3和Al(OH)3;
(3)为防止产品水解,故[Co(NH3)6]Cl3应在HCl氛围下蒸发浓缩、冷却结晶、减压过滤;
(4)若先加H2O2,将Co元素氧化到Co3+,后加氨水,会生成Co(OH)3,不利于产品的生成,故先加入氨水再加入H2O2,可防止Co(OH)3的生成,双氧水受热易分解,氨水温度过高会导致H2O2大量分解,降低产率,因此需水浴控温在50~60℃,温度不能过高;“氧化”步骤发生反应的离子方程式:H2O2+2Co2++2NH![]() +10NH3·H2O+6Cl-=2[Co(NH3)6]Cl3↓+12H2O;若无活性炭作催化剂,所得固体产物中除[Co(NH3)6]Cl3外还会有大量二氯化一氯五氨合钴[Co(NH3)5Cl]Cl2和三氯化五氨一水合钴[Co(NH3)5H2O]Cl3晶体,这体现了催化剂的选择性。
+10NH3·H2O+6Cl-=2[Co(NH3)6]Cl3↓+12H2O;若无活性炭作催化剂,所得固体产物中除[Co(NH3)6]Cl3外还会有大量二氯化一氯五氨合钴[Co(NH3)5Cl]Cl2和三氯化五氨一水合钴[Co(NH3)5H2O]Cl3晶体,这体现了催化剂的选择性。

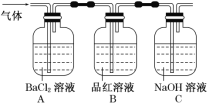
【题目】某同学用下列装置检验Cl2的性质。
|
|
|
Ⅰ |
| Ⅲ |
(1)I图中退色的是______(填“a”或“b”),I图烧杯中发生反应的离子方程式是______。
(2)Ⅱ图中的现象是_________。
(3)将铜丝换成铁丝,做Ⅱ实验,结果也能点燃,你认为铁丝也能点燃的理由是_______(填选项字母)。
A Fe与Cu都是金属元素 B Fe的熔点比Cu高
C Fe的密度比Cu小 D Fe的性质比Cu活泼
(4)将Ⅲ装置放置在光亮的地方(日光没有直接照射),一会儿后,量筒内黄绿色气体颜色变浅,量筒内液面上升等。(混合气中氢气含量为60%),己知:氢气含量超过52.8%,光照不会发生爆炸)
①量筒中液面上升的原因是_________。
②水槽用饱和食盐水而不用水的原因是_________。
【题目】现有部分前36号元素的性质或原子结构如下表
元素编号 | 元素性质或原子结构 |
R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
T | 基态原子3d轨道上有1个电子 |
X | |
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是________________________________________________________。
(2)S元素的化合价是否有正价?__________,原因是__________________________________,最外层电子排布式为________________________。
(3)T元素的原子N能层上电子数为__________,其原子结构示意图为__________。
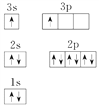
(4)X的核外电子排布图违背了__________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:____________________________________________________________________。
【答案】 氮原子2p轨道半充满,能量低,稳定 否 F的电负性最大,只能得电子 2s22p5 2 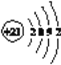 能量最低原理 电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量
能量最低原理 电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量
【解析】试题分析:R元素的基态原子最外层有3个未成对电子,次外层有2个电子,R是N元素;S元素的单质能与水剧烈反应,所得溶液呈弱酸性,S是F元素;T元素的基态原子3d轨道上有1个电子,T是21号元素Sc; X元素的原子核外有12个电子,X是Mg元素。
解析:根据以上分析,(1)R是N元素,氮原子2p轨道半充满,能量低,稳定,所以第一电离能要大于其同周期相邻的O元素。
(2)元素F的电负性最大,只能得电子,所以F元素没有正价;F元素的最外层电子排布式为2s22p5。
(3)Sc原子的核外电子排布式是1s22s22p63s23p63d14s2,所以N能层上电子数为2,其原子结构示意图为 。(4)根据能量最低原理,Mg原子最外层2个电子应排布在3s轨道上,所以核外电子排布图违背了能量最低原理。电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,所以燃放焰火时,焰火发出五颜六色的光。
。(4)根据能量最低原理,Mg原子最外层2个电子应排布在3s轨道上,所以核外电子排布图违背了能量最低原理。电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,所以燃放焰火时,焰火发出五颜六色的光。
【题型】综合题
【结束】
20
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图__________。
(2)写出Y元素最高价氧化物的水化物分别与HCl、NaOH溶液反应的离子方程式_______________________、_________________________。
(3)写出Z与Y的电子排布式______________、________________。
(4)元素T与氯元素相比,非金属性较强的是__________(用元素符号表示),下列表述中能证明这一事实的是__________。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两单质在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是__________(填元素符号),理由是________________________________________________。