题目内容
按照图1所示装置进行有关实验,打开分液漏斗玻璃塞,将A逐滴加入B中.
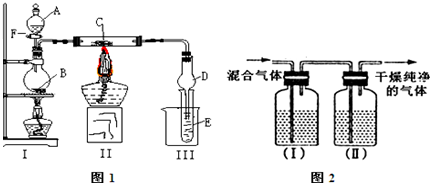
(1)①若A是浓盐酸,B为二氧化锰,当将A滴入B中时发生反应的离子方程式为 ,当实验一段时间后,发现C、D中有红棕色烟,则C的化学式为 .
②实验室常用MnO2与浓盐酸共热制取Cl2,也可用KClO3,KMnO4,K2Cr2O7代替MnO2与浓盐酸反应制Cl2.若制取等量的Cl2需浓盐酸最少的是 .
A.MnO2和浓盐酸反应 B.KClO3和浓盐酸反应
C.KMnO4和浓盐酸反应 D.K2Cr2O7和浓盐酸反应
③在实验室中,要获得干燥纯净的氯气,可以将它通过图2的装置,其中瓶I中盛放的是 .
(2)若A是乙醇,B是生石灰,实验中观察到C中黑色固体逐渐变红.当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到Ⅲ中试管壁出现了光亮的银镜.则 试管E中所发生反应的化学方程式 .
(3)①若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C与(2)相同.实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,则A是(写名称) .此实验中浓硫酸的作用是 .
②写出乙醇和A在浓硫酸存在并加热时所发生的反应方程式: ,此反应属于 .

(1)①若A是浓盐酸,B为二氧化锰,当将A滴入B中时发生反应的离子方程式为
②实验室常用MnO2与浓盐酸共热制取Cl2,也可用KClO3,KMnO4,K2Cr2O7代替MnO2与浓盐酸反应制Cl2.若制取等量的Cl2需浓盐酸最少的是
A.MnO2和浓盐酸反应 B.KClO3和浓盐酸反应
C.KMnO4和浓盐酸反应 D.K2Cr2O7和浓盐酸反应
③在实验室中,要获得干燥纯净的氯气,可以将它通过图2的装置,其中瓶I中盛放的是
(2)若A是乙醇,B是生石灰,实验中观察到C中黑色固体逐渐变红.当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到Ⅲ中试管壁出现了光亮的银镜.则 试管E中所发生反应的化学方程式
(3)①若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C与(2)相同.实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,则A是(写名称)
②写出乙醇和A在浓硫酸存在并加热时所发生的反应方程式:
考点:氯气的实验室制法,乙醇的化学性质,乙醛的银镜反应
专题:实验题,卤族元素,有机物的化学性质及推断
分析:(1)①二氧化锰与浓盐酸反应生成氯化锰、氯气、水.实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,即氯气与物质C反应生成FeCl3,据此判断物质C.
②2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O
MnO2+4HCl=MnCl2+Cl2↑+2H2O
KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
依据氧化还原反应电子守恒计算分析判断;
③氯气中含有氯化氢和水蒸气,可以通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
(2)乙醇和氧化铜反应生成乙醛铜和水,乙醛在水浴加热条件和银氨溶液反应生成单质银;
(3)①若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C与(2)相同.实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,说明A为甲酸在浓硫酸作用下脱水生成一氧化碳气体,一氧化碳气体通过氧化铜反应生成二氧化碳和铜,二氧化碳通过苯酚钠溶液生成苯酚变浑浊;
②乙醇和甲酸在浓硫酸作用下发生酯化反应生成甲酸乙酯和水;反应是取代反应;
②2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O
MnO2+4HCl=MnCl2+Cl2↑+2H2O
KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
依据氧化还原反应电子守恒计算分析判断;
③氯气中含有氯化氢和水蒸气,可以通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
(2)乙醇和氧化铜反应生成乙醛铜和水,乙醛在水浴加热条件和银氨溶液反应生成单质银;
(3)①若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C与(2)相同.实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,说明A为甲酸在浓硫酸作用下脱水生成一氧化碳气体,一氧化碳气体通过氧化铜反应生成二氧化碳和铜,二氧化碳通过苯酚钠溶液生成苯酚变浑浊;
②乙醇和甲酸在浓硫酸作用下发生酯化反应生成甲酸乙酯和水;反应是取代反应;
解答:
解:(1)①二氧化锰与浓盐酸反应生成氯化锰、氯气、水,反应离子方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,氯气与物质C反应生成FeCl3,故物质C为Fe;
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;Fe;
②2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O
MnO2+4HCl=MnCl2+Cl2↑+2H2O ;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
依据化学方程式和电子守恒计算判断得到生成等量氯气消耗KClO3最少;
故答案为:B;
③氯气中含有氯化氢和水蒸气,可以通过饱和食盐水除去氯化氢;
故答案为:饱和NaCl溶液;
(2)乙醇和氧化铜反应生成乙醛铜和水,乙醛在水浴加热条件和银氨溶液反应生成单质银,反应的化学方程式为:CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag↓+3NH3+H2O;
故答案为:CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag↓+3NH3+H2O;
(3)①若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C与(2)相同.实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,说明A为甲酸在浓硫酸作用下脱水生成一氧化碳气体,一氧化碳气体通过氧化铜反应生成二氧化碳和铜,二氧化碳通过苯酚钠溶液生成苯酚变浑浊;
故答案为:甲酸;脱水剂;
②乙醇和甲酸在浓硫酸作用下发生酯化反应生成甲酸乙酯和水,反应的化学方程式为:HCOOH+C2H5OH
HCOOC2H5+H2O;反应是取代反应,
故答案为:HCOOH+C2H5OH
HCOOC2H5+H2O; 取代(酯化)反应;
| ||
实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,氯气与物质C反应生成FeCl3,故物质C为Fe;
故答案为:MnO2+4H++2Cl-
| ||
②2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O
MnO2+4HCl=MnCl2+Cl2↑+2H2O ;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
依据化学方程式和电子守恒计算判断得到生成等量氯气消耗KClO3最少;
故答案为:B;
③氯气中含有氯化氢和水蒸气,可以通过饱和食盐水除去氯化氢;
故答案为:饱和NaCl溶液;
(2)乙醇和氧化铜反应生成乙醛铜和水,乙醛在水浴加热条件和银氨溶液反应生成单质银,反应的化学方程式为:CH3CHO+2Ag(NH3)2OH
| 水浴 |
故答案为:CH3CHO+2Ag(NH3)2OH
| 水浴 |
(3)①若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C与(2)相同.实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,说明A为甲酸在浓硫酸作用下脱水生成一氧化碳气体,一氧化碳气体通过氧化铜反应生成二氧化碳和铜,二氧化碳通过苯酚钠溶液生成苯酚变浑浊;
故答案为:甲酸;脱水剂;
②乙醇和甲酸在浓硫酸作用下发生酯化反应生成甲酸乙酯和水,反应的化学方程式为:HCOOH+C2H5OH
| 浓硫酸 |
| 加热 |
故答案为:HCOOH+C2H5OH
| 浓硫酸 |
| 加热 |
点评:本题考查了实验室制备氯气的实验装置和操作,试剂选择和除杂方法,物质性质的分析判断是解题关键,题目难度中等.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、非金属单质分子中一定含有非极性共价键 | ||||
| B、根据电离方程式:HCl=H++Cl-,判断HCl分子中存在离子键 | ||||
C、根据2C+SiO2
| ||||
| D、变化过程中化学键被破坏,不一定发生了化学变化 |
 尿素(H2NCONH2)可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)].
尿素(H2NCONH2)可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)].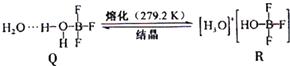
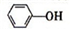 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子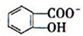 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)
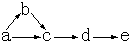 如图a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:其中:a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物.已知H2S在足量氧气中燃烧生成SO2.
如图a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:其中:a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物.已知H2S在足量氧气中燃烧生成SO2.