题目内容
经测定C3H7OH和C6H12组成的混合物中碳的质量分数为78%,则此混合物中氧的质量分数是( )
| A、8% | B、10% |
| C、22% | D、18% |
考点:元素质量分数的计算
专题:计算题
分析:C3H7OH可以将写成C3H6?H2O,根据混合物中碳的质量分数为78%,计算出(CH2)的质量分数,再结合化学式计算出C3H6?H2O和C6H12中所H2O在混合物中的质量分数,从而求出混合物中氧的质量分数是.
解答:
解:混合物中碳的质量分数为78%,所以(CH2)的质量分数为:
=0.91,所以水的质量分数为1-0.91=0.09,所以则此混合物中氧的质量分数是0.09×
=8%,
故选8%.
| 78% | ||
|
| 16 |
| 18 |
故选8%.
点评:本题考查质量分数的计算,难度中等,关键根据碳的质量分数结合C3H7OH化学式计算混合物中(CH2)质量分数.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
下列有关反应限度的叙述正确的是( )
| A、大多数化学反应在一定条件下都有一定的限度 |
| B、依据焓判据:NH4HCO3受热分解可自发进行 |
| C、使用催化剂,可降低反应的活化能,加快反应速率,改变反应限度 |
| D、FeCl3与KSCN反应达到平衡时,向其中滴加KCl溶液,则溶液颜色变深 |
将乙炔通入苯和甲醛形成混合溶液,测得此混合溶液中碳的质量分数为a,则该混合物中氧的质量分数为( )
A、1-
| ||||
B、1-
| ||||
C、
| ||||
D、
|
元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法不合理的是( )
| A、由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| B、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| C、在元素周期表中,硅、锗都位于金属与非金属的交界处,都可以作半导体材料 |
| D、Cs和Ba分别位于第六周期ⅠA族和ⅡA族,碱性:CsOH>Ba(OH)2 |
下列说法错误的是( )
| A、一般的水是由10个以上的水分子聚结组成一个水分子团,叫大分子团水,科学家能把大分子团水变成5-8个水分子组成的小分子团水,一次饮用125mL可维持人体6小时正常需水量,这个转变过程改变了水分子间的结构和物理性质 |
| B、离子化合物中可能有共价键 |
| C、科学家在青藏高原深处发现了天然的氮化硼(BN,具有高熔点、高密度、高硬度等特性),它可能是原子晶体 |
| D、用“撕裂”方法可从石墨材料中剥离出的单层碳原子面材料(石墨烯),用这种方法从C60、金刚石等碳原子中获得“只有一层碳原子厚的碳薄片”也将成为研究方向 |
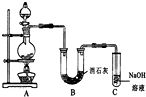 某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应).
某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应).