题目内容
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 是四种短周期元素,
是四种短周期元素,![]() 、
、![]() 、
、![]() 同周期,
同周期,![]() 、
、![]() 同主族。
同主族。![]() 的原子结构示意图为
的原子结构示意图为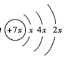 ,
,![]() 、
、![]() 形成的化合物的电子式为
形成的化合物的电子式为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.原子半径:![]()
B.电负性:![]()
C.原子序数:![]()
D.最高价氧化物对应水化物的酸性:![]()
【答案】D
【解析】
由A的原子结构示意图可知,x=2,A的原子序数为14,故A为Si元素;由b与c形成的化合物的电子式可知c原子核外应有5个电子,为第ⅤA族元素,应为N元素,b最外层应有1个电子,与a同周期,应为Na元素,c、d同主族,则d为P元素;
A.根据半径变化规律,同周期从左到右半径减小,同主族从上到下半径增大,原子半径应为Na>Si>P>N,即b>a>d>c,故A错误;
B. 同周期元素从左到右元素的电负性逐渐增强,同主族元素从上到下电负性逐渐减弱,故电负性N>P>Si>Na,则应为c>d>a>b,故B错误;
C. 原子序数的大小顺序为P>Si>Na>N,即d>a>b>c,故C错误;
D. 元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,为N>P>Si,即c>d>a,故D正确。
答案选D。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取M g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取50.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取50.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。
实验中所记录的数据如下表:
滴定次数 实验数据 | 1 | 2 | 3 | 4 |
待测溶液体积/mL | 50.00 | 50.00 | 50.00 | 50.00 |
滴定管初读数/mL | 0.00 | 0.20 | 0.10 | 0.15 |
滴定管末读数/mL | 20.95 | 21.20 | 20.15 | 21.20 |
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和_______、________。
(2)操作I为______________,操作Ⅱ为______________。
(3)在方案Ⅱ中滴定终点的判断方法是_______________________________。
(4)在方案Ⅱ中发生的离子反应方程式为____________________________。
(5)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为___________。(写成分数形式)
(6)方案Ⅱ中氧化还原滴定过程中,导致待测液Na2SO3浓度变小的是_____(填序号)。
a.用碱式滴定管量取50mL待测液过程时,开始仰视,滴定结束时俯视
b.用碱式滴定管量取50mL待测液过程时,一开始有气泡,滴定结束后没气泡
c.酸式滴定管用蒸馏水润洗后,没有用酸性KMnO4溶液多次润洗
d.锥形瓶用蒸馏水润洗后,直接装50.00mL的待测液
e.滴定过程时,开始时平视,滴定结束时仰视
【题目】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。其中J为0族元素。
X | Y | Z | |
R | |||
W | |||
J |
下列说法正确的是( )
A.基态R原子的轨道表示式为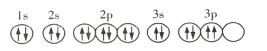
B.![]() 与
与![]() 的半径大小关系为
的半径大小关系为![]()
C.Y的第一电离能大于X的第一电离能
D.X、Y、Z、R、W中,电负性最大的元素为W