题目内容
下列判断正确的是( )
| A、元素周期表中查得的相对原子质量为同位素的相对原子质量 |
| B、化学键的变化一定会引起化学反应的变化 |
| C、只含有共价键的物质一定是共价化合物 |
| D、全部由极性键构成的分子不一定是极性分子 |
考点:元素周期表的结构及其应用,化学键
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:A.周期表中为元素的相对原子质量;
B.化学变化中一定有化学键断裂和生成;
C.只含有共价键的物质,可能为单质;
D.全部由极性键构成的分子,可能为非极性分子.
B.化学变化中一定有化学键断裂和生成;
C.只含有共价键的物质,可能为单质;
D.全部由极性键构成的分子,可能为非极性分子.
解答:
解:A.周期表中为元素的相对原子质量,由同位素的相对原子质量及其丰度计算得到,故A错误;
B.化学变化中一定有化学键断裂和生成,而化学键的变化不一定会引起化学反应的变化,如HCl溶于水,故B错误;
C.只含有共价键的物质,可能为单质,如氯气只含共价键,故C错误;
D.全部由极性键构成的分子,可能为非极性分子,如甲烷;也可能为极性分子,如HCl,故D正确;
故选D.
B.化学变化中一定有化学键断裂和生成,而化学键的变化不一定会引起化学反应的变化,如HCl溶于水,故B错误;
C.只含有共价键的物质,可能为单质,如氯气只含共价键,故C错误;
D.全部由极性键构成的分子,可能为非极性分子,如甲烷;也可能为极性分子,如HCl,故D正确;
故选D.
点评:本题考查周期表的结构及应用、化学键等,为高频考点,把握物质中的化学键及化学键与分子极性、化学变化的关系为解答的关键,注重基础知识的考查,选项A为解答的难点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于钠的叙述中错误的是( )
| A、钠燃烧时发出黄色火焰,生成Na2O2 |
| B、钠投入CuSO4溶液中能生成红色的铜 |
| C、钠原子最外层有一个电子,具有强还原性 |
| D、钠与H2O反应能产生H2 |
下列微粒既具有氧化性又具有还原性的是( )
①Al3+ ②Cl- ③N2 ④MnO4- ⑤CO2 ⑥H2O2 ⑦Fe2+ ⑧MnO42-.
①Al3+ ②Cl- ③N2 ④MnO4- ⑤CO2 ⑥H2O2 ⑦Fe2+ ⑧MnO42-.
| A、①④⑤⑦ | B、③⑥⑦⑧ |
| C、④⑤⑥⑧ | D、①②③⑥ |
下列有关原子结构和元素周期律的表述中不正确的是( )
①原子序数为l5的元素的氢化物为三角锥形
②ⅦA族元素是同周期中非金属性最强的元素
③第三周期ⅣA族元素的原子核电荷数和中子数均为6
④原子序数为26的元素位元素周期表的第四周期第ⅧB族.
①原子序数为l5的元素的氢化物为三角锥形
②ⅦA族元素是同周期中非金属性最强的元素
③第三周期ⅣA族元素的原子核电荷数和中子数均为6
④原子序数为26的元素位元素周期表的第四周期第ⅧB族.
| A、①② | B、①③ | C、②④ | D、③④ |
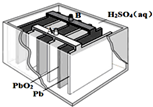 铅蓄电池是最常见的二次电池,其构造示意图如图.发生反应的化学方程式为:
铅蓄电池是最常见的二次电池,其构造示意图如图.发生反应的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)
| 放电 |
| 充电 |
| A、放电时,正极反应为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-═PbSO4(s)+2H2O(l) |
| B、铅蓄电池广泛用于汽车启动电源,可以边使用边充电,充电时,应将充电电源的正极与铅蓄电池的接线柱A相接 |
| C、实验室用铅蓄电池做电源精炼粗铜时,应将粗铜与接线柱B相连接 |
| D、铅蓄电池做电源电解AgNO3溶液,当有标况下11.2升O2产生时,消耗2mol H2SO4 |
