题目内容
在周期表中氧化性最强的一族元素是 ,它们的原子最外电子层上的电子数目是 ,该族元素随核电荷数的递增,原子半径逐渐 ,阴离子还原性逐渐 .
考点:卤素原子结构及其性质的比较,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:同一周期元素中,元素的非金属性随着原子序数的增大而增强,同一主族元素中,元素的非金属性随着原子序数的增大而减弱,元素的非金属性越强,其氧化性越强;同一主族元素,随着原子序数的增大,其单质的氧化性逐渐减弱,阴离子的还原性逐渐增强,原子半径逐渐增大.
解答:
解:同一周期元素中,元素的非金属性随着原子序数的增大而增强,同一主族元素中,元素的非金属性随着原子序数的增大而减弱,元素的非金属性越强,其氧化性越强,所以在周期表中氧化性最强的一族是卤族元素,其最外电子层上有7个电子,该族元素随着核电荷数的递增,原子核对最外层电子的吸引能力逐渐减小,则原子半径逐渐增大,阴离子的还原性逐渐增强,故答案为:卤族元素;7;增大;增强.
点评:本题以卤族元素为载体考查了同一主族元素性质的递变性,熟悉元素周期律知识即可解答,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、凡分子组成符合Cn(H2O)m的化合物属糖类 |
| B、有甜味的物质一定属于糖类 |
| C、糖类可看做是碳的水化物 |
| D、糖类物质在空气中燃烧都生成CO2和H2O |
下列判断正确的是( )
| A、元素周期表中查得的相对原子质量为同位素的相对原子质量 |
| B、化学键的变化一定会引起化学反应的变化 |
| C、只含有共价键的物质一定是共价化合物 |
| D、全部由极性键构成的分子不一定是极性分子 |
下列各组溶液中,离子一定能大量共存的是( )
| A、强碱溶液中:Na+、Mg2+、SO42-、AlO2- |
| B、某无色溶液中:NH4+、Fe3+、MnO4-、NO3- |
| C、含有0.1mol/L Fe3+溶液中:K+、Mg2+、Cl-、SCN- |
| D、与铝反应生成H2的溶液中:Na+、K+、Cl-、SO42- |
能以离子键相结合生成AB型(B为阴离子)离子化合物,它们的原子序数分别为( )
| A、11和17 | B、11和16 |
| C、20和9 | D、13和17 |
在一支量程为20mL的酸式滴定管中盛放盐酸,液面恰好在a mL刻度处,把管内液体全部放出,所得液体体积是( )
| A、a mL |
| B、(20-a)mL |
| C、大于(20-a)mL |
| D、大于a mL |
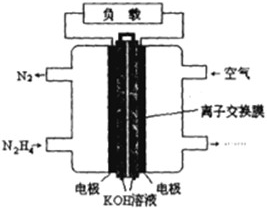 肼(N2H4)是火箭发射常用的燃料.
肼(N2H4)是火箭发射常用的燃料.