题目内容
【题目】有关对食盐叙述错误的是
A.可作食品调味剂
B.可作食品防腐剂
C.可作氯碱工业和纯碱工业的原料
D.电解饱和食盐水可得到金属钠
【答案】D
【解析】
食盐常用于调味品,可使细胞脱水而起到防腐剂的作用,工业常用于氯碱工业制备氯气、氢气和氢氧化钠,也常用于纯碱工业,以此解答。
A.Na为人体不可缺少的元素,食盐可用于食品调味剂,具有咸味,A正确;
B.食盐可使细胞脱水而起到防腐剂的作用,B正确;
C.工业电解饱和食盐水制备氯气、氢气和氢氧化钠,用食盐、氨气、二氧化碳制备纯碱,C正确;
D.钠性质活泼,与水剧烈反应,电解食盐水不能制得钠,应电解熔融氯化钠,D错误;
故合理选项是D。

 名校课堂系列答案
名校课堂系列答案【题目】下列递变规律不正确的是( )
A.Na、Mg、Al原子的失电子能力逐渐减弱
B.Si、P、S元素的最高正化合价依次降低
C.C、N、O的原子半径依次减小
D.Cl、Br、I的气态氢化物的稳态性依次减弱
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡常数(Ka) | 7.2×10﹣4 | K1=4.4×10﹣7 | 3.0×10﹣8 |
(1)将浓度为0.1molL﹣1 HF溶液加水稀释一倍(假设温度不变),下列各量增大的是 .
A.c(H+)
B.c(H+)c(OH﹣)
C.![]()
D.![]()
(2)25℃时,在20mL 0.1molL﹣1氢氟酸中加入V mL 0.1molL﹣1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 . 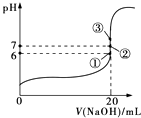
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F﹣)﹣c(Na+)=9.9×10﹣7 molL﹣1
C.②点时,溶液中的c(F﹣)=c(Na+)
D.③点时V=20mL,此时溶液中c(F﹣)<c(Na+)=0.1molL﹣1
(3)物质的量浓度均为0.1molL﹣1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液.依据数据判断pH由大到小的顺序是 .
(4)Na2CO3溶液显碱性是因为CO32﹣水解的缘故,请设计简单的实验事实证明之 .
(5)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H﹣O﹣F.HFO与水反应得到HF和化合物A,每生成1mol HF转移mol电子.